
心脏手术前粪便隐血筛查
Takami et al.
**中文内容仅供参考,一切以英文原文为准。
简介
消化道出血仍然是心脏手术后主要的并发症之一,尤其是经历了体外循环(CPB)的案例。虽然这种情况相对罕见,但却可能大幅增加术后死亡率。从2002年的0.75%增加到2011年的1.95%,胃肠道出血的发生率随时间增加,可能是由于心脏手术的复杂性、患者年龄和合并症的增加。据在非手术人群中的报道,胃肠出血也可能与抗血小板(包括阿司匹林)和口服抗凝剂(包括直接作用口服抗凝剂(DOACs)和华法林)的使用增加有关。此外,伴有出血的活动性胃肠道肿瘤使心脏手术患者的围手术期管理和手术策略更具挑战性。
根据最近的报道,心脏手术后消化道出血的术前危险因素包括年龄> 70岁、射血分数< 35%、充血性心力衰竭、既往消化道疾病、房颤、肝胆胰功能障碍、肾脏疾病和慢性阻塞性肺疾病。然而,从未讨论过术前检查胃肠道出血或出血性胃肠道癌。本文作者探讨了粪便免疫化学试验(FIT)术前筛查粪便隐血的临床作用,该方法已广泛用于检测胃肠道出血和结直肠癌。
材料和方法
研究的病人
本回顾性研究于2012年1月至2020年12月在藤田卫生大学医院进行了连续1732例择期心胸主动脉手术患者的观察,经过了相关委员会的批准。
术前FIT
根据患者的依从性,术前约2 - 3周在门诊进行1 - 2次术前FIT检查,使用全自动粪便潜血检测系统(HM-JACKarc,Minaris Medical Co., Ltd.,东京,日本),当时尚未因手术暂停服用抗血小板和抗凝药物。采样后,患者立即提交粪便,即使不能立即提交样本,也在提交前较短的时间内将粪便储存在冰箱中。一次FIT筛查一个粪便样本,成本< 10美元。阳性FIT的截止值为> 30 μg血红蛋白/g粪便,定量为1+为31-150 μg,2+为151-450μg,3+为≥ 451 μg。所有FIT阳性的患者由肠胃科医生决定是否进行胃镜检查和/或结肠镜检查。
数据收集
从医院数据库中回顾性地收集临床资料,还从医院图表中获得了内镜检查的程序数据,包括带有病理结果和程序细节的电子报告,以确认胃肠道病变的诊断。在进行了内窥镜干预的病例中,收集了内窥镜手术类型的详细信息。
统计分析
连续变量表示为平均值±标准差。采用Levene方差检验。连续变量采用Mann - Whitney U检验,分类变量采用Fisher精确检验对术前fits阳性和阴性患者进行统计学分析。双侧p值< 0.05认为有统计学意义。采用多变量logistic回归分析,对p值< 0.10的变量进行调整后,确定术前FITs阳性的预测因素。给出最终回归模型中每个自变量的比值比(OR)和95%置信区间(CI)。所有的统计分析都是通过网站(http:// www.jichi.ac.jp/sa)上的统计软件“EZR”(Easy R)进行的。
结果
FIT总体结果(表1和图1)
在1732例择期手术患者中,1663例(96%)接受术前FIT筛查。其中出现1次或者2次 FIT阳性的有227例(13.7%)。在FIT阳性患者中,有54例(23.8%)一轮FIT一次阳性,113例(49.8%)二轮FIT一次阳性, 60例(26.4%)两轮FIT均为阳性。两组FIT均为阳性患者粪便血红蛋白含量(240 ± 204 μg/g)显著高于一组FIT阳性患者(170 ±180和173 ± 186 μg/g, p =0.023)。
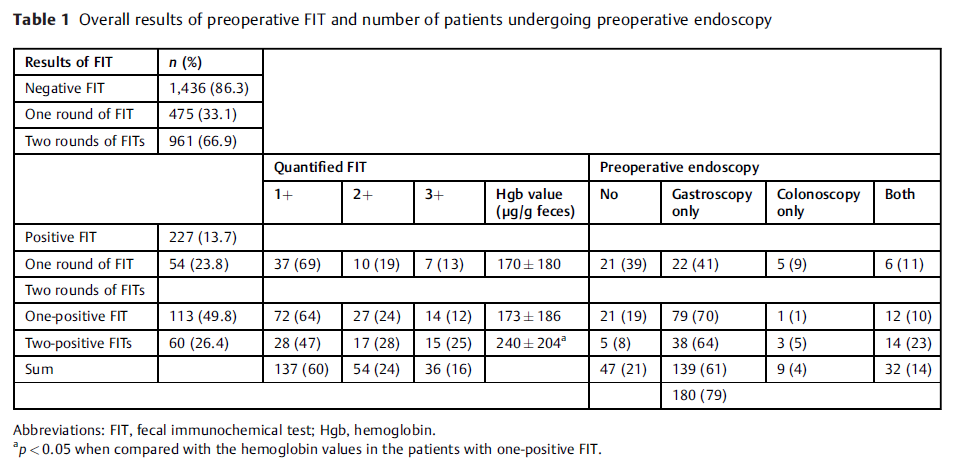
表1. 术前FIT筛查结果。
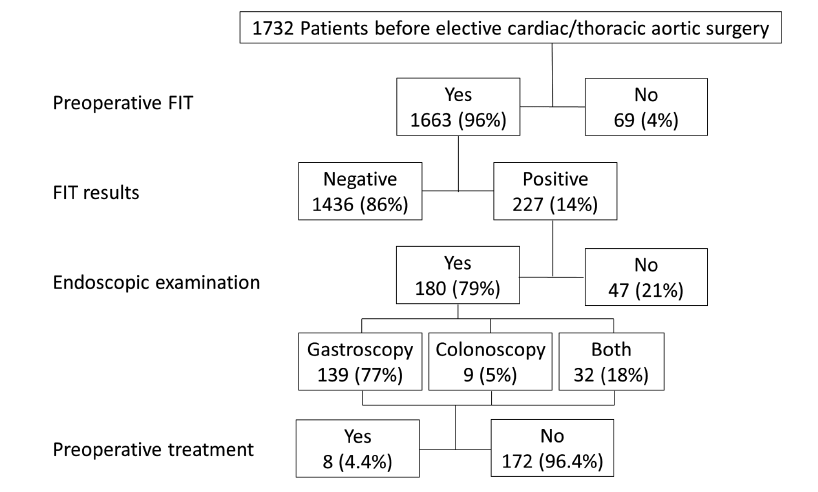
图1. 术前FIT筛查流程图。
患者特征(表2和表3)
FIT阳性患者明显比阴性患者年龄大(72±9 VS 67±12岁,p=0.0007),胸X光片心胸比更高(53.4 ± 7.0% VS 51.9 ± 6.6%, p=0.006),心电图房颤更频繁(19% VS 11%,p=0.002)。在FIT阳性患者中,既往胃肠道疾病占主导地位(23% VS 16%,p = 0.023),同时伴有慢性肾脏疾病更为常见(38% VS 28%,p = 0.002)。在用药方面,质子泵抑制剂(PPI)的使用差异无统计学意义。然而,抗凝剂(24% VS 16%,p=0.004),特别是DOACs(15% VS 6%,p=0.001)的使用频率更高,但是抗血小板药物的使用率没有显著差异。
在多因素logistic回归分析中,在调整年龄、胃肠道病史、慢性肾脏疾病、胸片心胸比、房颤、抗凝剂和抗血小板后,FIT阳性的独立预测因子为年龄> 70岁(OR 1.86, 95% CI 1.020-1.060;p < 0.001), DOAC使用(OR 1.57, 95% CI 1.031-2.342; p=0.04),慢性肾脏疾病(OR 1.38, 95% CI 1.010-1.870;P = 0.03)。合并这些变量的模型的受试者工作特征曲线下面积为0.77 (95% CI 0.66-0.88)。
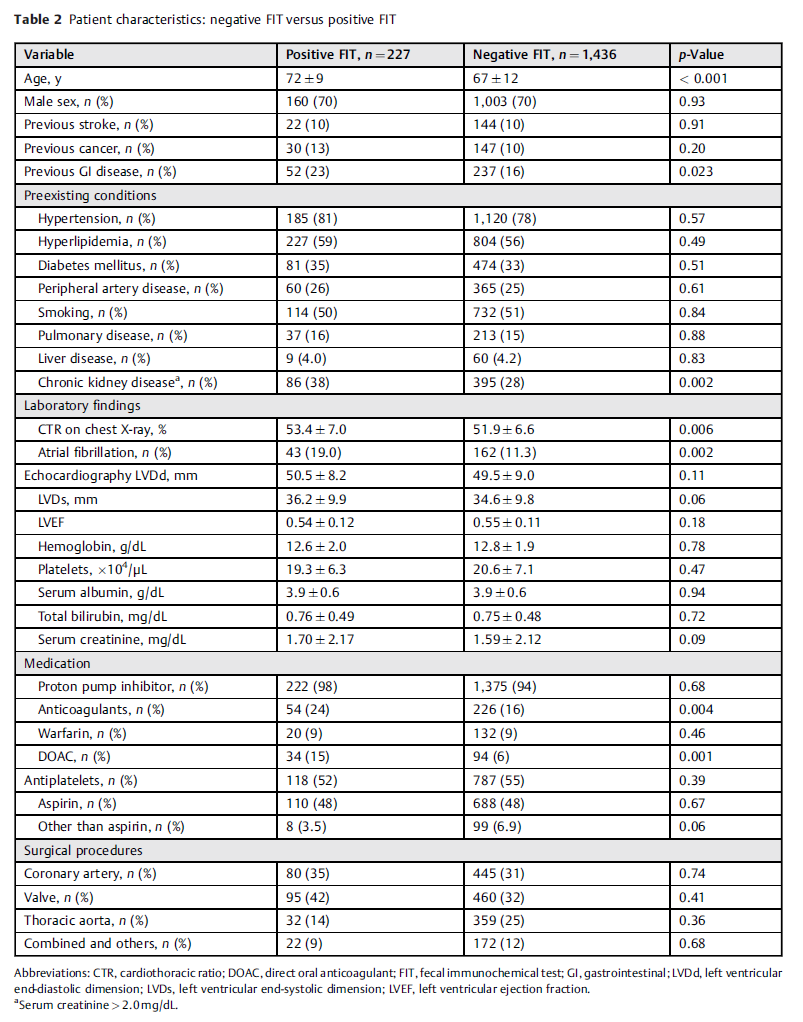
表2. 患者基线特征。
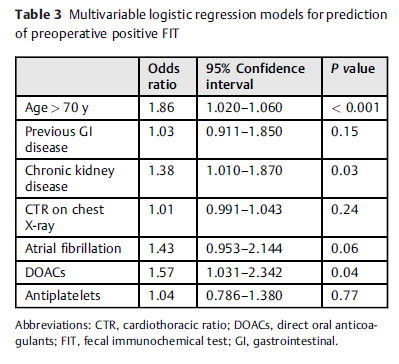
表3. 多变量逻辑回归模型用于预测术前FIT阳性。
术前内镜检查(表1)
在227例FIT阳性患者中,180例(79%)接受了术前内镜检查,包括胃镜139例(61%),结肠镜9例(4%),两者均有32例(14%)。进行胃镜和结肠镜检查的有6名患者(一轮FIT一次阳性患者的11%)加26名患者(两轮FIT阳性患者的33%)。尽管FIT呈阳性,但1轮FIT 1次阳性的21例患者, 2轮FIT 2次阳性的5例患者未进行任何类型的内镜检查。
内窥镜检查结果(图2)
FIT阳性患者术前胃镜检查最常见的发现是萎缩性胃炎(n=102/286,36%),其次是反流性食管炎(n=43,15%),裂孔疝(n=36,13%),贲门息肉(n=25,9%)和Barrett食管(n=21,7%),不过未发现出血性溃疡或出血病变。次要的发现展示在图2,其中胃癌2例(1.2%)。
FIT阳性患者术前结肠镜检查(n=49)结果有结肠多发性息肉(n=12,25%)、结肠息肉(n=8,17%),其次为憩室(n=7,15%)、盲肠息肉(n¼5,10%),未见异常(n=4,8%)。次要的发现展示在图2,包括结直肠癌5例(12%),缺血性结肠炎(1例),艰难梭菌结肠炎(1例)。但未检出活动性出血病变。
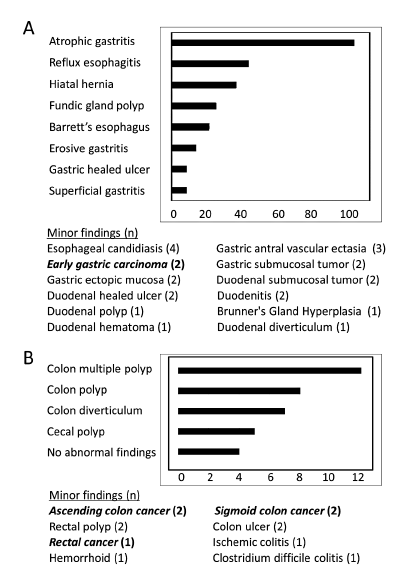
图2. FIT阳性患者的术前镜检查的主要发现 (A) 胃镜检查 (B) 结肠镜检查。特别指出,有2例早期胃癌患者和5例结直肠癌患者。
术前胃肠道治疗(表4)
180例检查FIT阳性术前行内镜患者中,8例(4.4%)术前接受胃肠治疗以控制出血。7例患者接受息肉切除术,其中3例在病理上诊断为结肠癌。在其中两个病例中,选择了非体外循环冠状动脉旁路移植术,后行结肠切除术,以避免CPB相关的结肠癌出血和CPB对免疫系统的抑制。其中一例,由于担心低温CPB下结肠癌出血,推迟了心脏手术,先进行内镜粘膜切除术(EMR),然后进行全弓置换术。对于在结肠镜诊断为艰难梭菌(CD)结肠炎的一位患者,进行二尖瓣修复前给予了口服万古霉素治疗22天。
术后胃肠道事件及治疗(表5)
180例术前行内镜检查的FIT阳性患者中,有28例(15.6%)出现术后GI事件或接受了GI治疗。其中21例(75%)患者接受了癌症相关治疗。2例术前诊断为早期胃癌的患者在心脏手术后行内镜下粘膜下剥离(ESD)。
3例术前胃镜检查出萎缩性胃炎的患者发现术后胃十二指肠溃疡性出血。其中一人在主动脉瓣置换术和升主动脉置换术后患上急性胰腺炎,在医院死亡。术前诊断为多发结肠息肉的14例患者中,6例术后行息肉切除术,病理呈癌阴性。9例肿瘤病理阳性患者术后行结肠切除术或直肠切除术,3例肿瘤阳性患者术后行ESD或EMR。2例术前结肠镜检查未发现异常的患者出现憩室出血,使用药物治疗或行结肠切除术。此外,1例术后CD结肠炎患者和1例非闭塞性肠系膜缺血(NOMI)患者术后死亡。
术前FIT阴性的1436例患者中,术后出现胃肠道并发症的21例(1.46%)明显少于术前FIT阳性的28例(12.3%,p < 0.001)。FIT阴性患者的胃肠道病变包括NOMI (n=6,29%)、下消化道出血(n=6,29%)、胃十二指肠溃疡引起的上消化道出血(n=5,24%)、胆道疾病(n=2)、肠梗阻(n=1)和CD结肠炎(n=1),均与癌症无关。
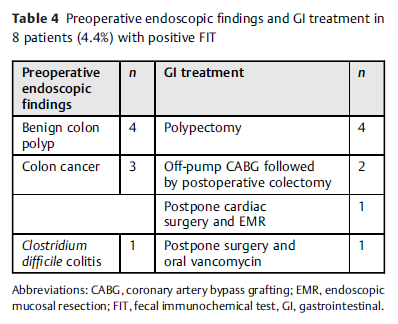
表4. 术前胃肠道的治疗(8名接受内镜检阳性FIT患者)。
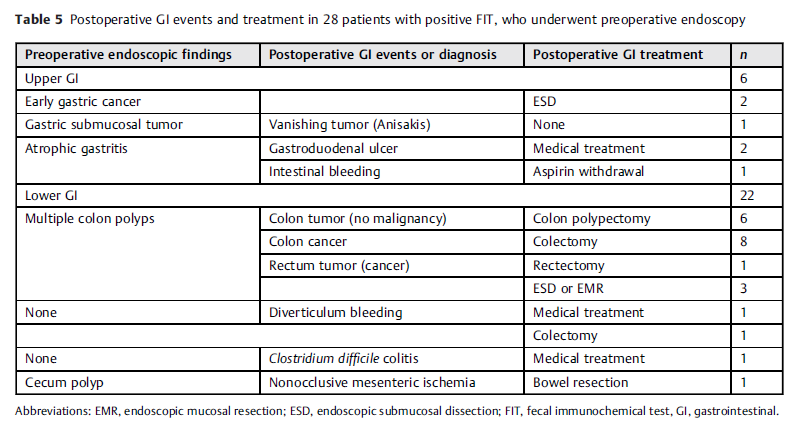
表5. 术后胃肠道并发症及治疗情况(28个经历了内镜检的FIT阳性患者)。
讨论
本文作者提供的是心脏手术前FIT筛查的首次报告,主要发现以下三个要点:
1.术前FIT阳性与心脏手术候选患者的年龄、DOAC使用和慢性肾脏疾病密切相关。
2. FIT阳性患者术后胃肠道事件发生率高于FIT阴性患者。
3.术前FIT可能有助于发现胃肠道恶性病变,因此适当调整手术风险、手术策略和术后管理。
总的来说,FIT通过一种对结直肠癌具有高灵敏度和特异性的血红蛋白特异性抗体来检测粪便样本中的溶血。由于大规模的FIT筛查可以降低晚期结直肠癌的发病率,因此大多数指南建议在没有症状的50岁人群中开始进行FIT筛查。除结直肠癌外,FIT阳性还与其他胃肠道疾病有关,包括结直肠憩室、炎症性肠病、痔疮、上消化道癌、食管炎和消化性溃疡。基于这些背景,本文作者术前进行FIT筛查,以评估各种胃肠道病理引起的消化道出血的手术风险。
然而,50%以上的FIT阳性患者结肠镜检查结果为阴性。影响FIT表现的变量之一是抗凝血剂和阿司匹林的使用。低剂量阿司匹林服用者每1000人年的上消化道和下消化道出血发生率分别为0.97和1.68,而非阿司匹林服用者分别为0.67和0.76。尽管大多数FIT筛查指南不建议停用抗血小板和抗凝血药物,但挪威的一项大型队列研究显示,阿司匹林和DOAC使用者对结直肠癌的阳性预测值较低,特别是对于DOAC使用者,FIT结果阳性后结肠镜检查发现显著病变的比例较低。这一发现与本文作者的结果相一致,FIT阳性患者中使用DOAC的患者比例明显更高。即DOAC使用者假阳性FIT的风险增加。虽然胃镜对FIT阳性的作用也存在争议,但有报道称,在结肠镜“阴性”的FIT阳性患者中,胃镜对胃炎、消化性溃疡疾病和胃癌的诊断率很高。
Hess等报道,10,285例心脏手术后最常见的胃肠道并发症是CD感染(28%),其次是肝功能衰竭(22%)和胃肠道出血(20%)。Elgharably等人也报道了29909例心脏外科手术中消化道并发症发生率为3.5%,住院死亡率为14%。消化道出血被认为是最常见的致命消化道并发症,消化道出血最常见的病因是胃和十二指肠溃疡。他们的发现与Krawiec等人之前的报告一致,9017例患者中发现了91例需要内镜检查的消化道出血事件,其中上消化道来源、十二指肠溃疡或应激性胃炎占78%。在本文作者的研究患者中,术后胃肠道事件低于这些研究,可能是由于围手术期PPI使用率较高。
在本文作者的研究中,术前FIT对胃肠道出血部位的识别作用不大,尽管很多FIT阳性患者接受了胃镜检查(与结肠镜检查相比,胃镜检查更容易被接受,因为它的侵入性更小)。由于使用抗凝和抗血小板药物的患者存在FIT假阳性的风险,因此在这些患者中是否应进行术前胃镜或结肠镜检查是有争议的。
除了上述的术前消化道状况,术后情况,如全身灌注不足和内脏血管收缩,可能导致粘膜缺血,导致术后消化道出血。总之,围手术期使用PPI对于避免术后消化道出血可能是最重要的。此外,术前FIT筛查面临的困难有不断增加的紧急手术和患者的依从性。
然而,本文作者的研究表明术前FIT可能有助于发现胃肠道恶性病变,特别是结直肠癌。如表4和表5所示,10.6%的FIT阳性患者在心脏手术前后接受了胃肠道癌症治疗,而FIT阴性患者术后出现非癌症相关胃肠道并发症的比例仅为1.46%。在伴有恶性肿瘤的患者中,麻醉和手术决策更具挑战性。由于一期手术(即同时进行心脏手术和胃肠道癌症治疗)对胃肠道癌症患者的出血风险较高,因此,在心脏手术后2个月内安排癌症治疗可能更合适,尽量避免癌症治疗延迟带来的风险。CPB对免疫系统的抑制和癌症的进展也有一定的影响。虽然报道的合并心脏病和活动性癌症患者的发病率从3.4%到7%不等,但由于人口老龄化,这种合并症的患病率正在增加。因此,术前FIT筛查胃肠道恶性肿瘤在心脏外科患者,尤其是复杂、高危的心脏外科患者中发挥着重要作用。结直肠癌可能引起的菌血症或脓毒症也引起了人们的关注。一项荟萃分析显示,49%的牛链球菌心内膜炎或败血症患者发生结直肠癌在> 65岁的老年人群中,结直肠癌诊断前后感染性心内膜炎的流行病学发病率明显高于肺癌、乳腺癌和前列腺癌。结直肠癌患者的人工瓣膜心内膜炎是外科关注的问题。术前FIT检测结直肠癌有一定的临床意义。
研究局限性
首先,本研究的局限性在于其回顾性设计和研究人群的规模。其次,由于患者的依从性,一些患者术前进行了两次FITs,而另一些患者只进行了一次。一轮FIT阳性患者的内镜检查率较低,可能会影响结果。第三,FIT阳性的患者进行了各种检查,这取决于咨询的胃肠科医生的临床决定。很少有人做了完整的内窥镜检查。第四,虽然本文作者发现FIT阳性与抗凝药物的使用密切相关,但没有关于华法林和DOAC患者抗凝的实验室状态的数据。
结论
心脏手术前FIT筛查,受年龄、DOAC使用及慢性肾脏疾病的影响,对识别消化道出血部位意义不大。然而,在一些患者中,它对发现胃肠道恶性病变具有重要作用,可能影响手术风险、手术策略和术后管理。考虑到DOAC患者的FIT假阳性,对于只有一次FIT阳性的患者,观察可能是可以接受的,而对于两次FIT阳性的患者,可能需要进行诊断性内窥镜检查,特别是结肠镜检查以发现恶性肿瘤。
评价
本研究是对心脏手术前FIT筛查的首次全面报告,为临床医生在心脏手术前的风险评估和管理提供了宝贵的数据支持。尽管存在人群相关的局限性,但其结果强调了FIT筛查在心脏手术患者中的潜在价值,特别是在识别胃肠道恶性肿瘤方面,有助于更好的改善心脏手术前的临床路径和患者管理策略。
本期中文内容
王昕宇
/初稿
涂 治
/初审
范成铭
/校审
范成铭,博士
The Thoracic and Cardiovascular Surgeon 编委
中南大学湘雅二医院
外科学博士,药学博士后,副研究员,博士研究生导师,中南大学湘雅二医院心血管外科主治医师,中华志愿者协会中西医结合专家志愿者委员会心外科专业组常务委员,中国研究型医院学会心脏瓣膜病专业委员会青年委员,湖南省医学会胸心血管外科学专业委员会青年委员,美国阿拉巴马大学伯明翰分校生物医学工程学系国家公派联合培养博士,中南大学十佳大学生、中南大学湘雅二医院青年岗位能手、十佳青年、湖南省卫生健康高层次人才,中南大学“升华学者计划”优秀青年人才。美国胸外科协会(AATS) Evarts A. Graham Memorial Traveling Fellowship 2023年获得者(首位获得该奖项的国内心外科医生,每年仅资助一名心外科医师)。美国Samuel and Jean Frankel心血管中心Fellow。荷兰Catharina医院心胸外科Fellow,比利时Cliniques universitaires Saint-Luc医院心胸血管外科Fellow。主持国家自然科学基金2项、湖南省优秀青年科研基金、湖南省优秀博士后基金各1项,先后获省优秀博士研究生学位论文奖、湖南省医学科技一等奖2项,科技进步二等奖1项,医学十大临床创新技术奖1项。主要研究方向为缺血性心脏病的细胞相关治疗研究,以第一或通讯作者身份在国内外学术期刊发表学术论文30余篇,现担任SCI期刊:Journal of the Renin-Angiotensin-Aldosterone System主编、Clinical and Experimental Hypertension主编,Journal of Cardiothoracic Surgery、BMC Bioinformatics副主编,Clinical Case Reports高级主编,European Journal of Medical Research副主编及心脏病学栏目主编,BioMed Research International、PLoS ONE、PeerJ学术主编,BMC Medicine、Reviews in Cardiovascular Medicine、Thoracic and Cardiovascular Surgeon、BMC Cardiovascular Disorders等多本SCI杂志编委。
德国胸心血管外科学会会刊。
The Thoracic and Cardiovascular Surgeon 发表来自国际公认的胸心血管外科医师、心脏病学家、麻醉学家、生理学家和病理学家的最高标准文章。本刊是这一领域工作者的重要资源。
原创论文、简讯、综述和重要会议公告将报告关键的临床进展,同时为读者提供心血管和胸外科的理论背景。病例报告在我们的开放获取姊妹期刊The Thoracic and Cardiovascular Surgeon Reports上发表。
