
胸腺癌相关的重症肌无力:一份病例报道
Lopes et al.
**中文内容仅供参考,一切以英文原文为准。
重症肌无力和胸腺瘤常常同时出现,约有10%的肌无力患者同时伴有胸腺瘤。胸腺癌是人类最为罕见/最具侵袭性的上皮肿瘤之一,迄今为止与重症肌无力的关联尚不明确。本文的临床病例以及文献综述介绍了关于胸腺癌(无胸腺瘤迹象)与重症肌无力(乙酰胆碱受体抗体阳性)之间罕见的关联性。胸腺切除术后两年,患者的临床症状基本改善,预后良好。该病例提示胸腺癌可能与重症肌无力有关,从肿瘤学和神经病学的角度来说,该类患者可能会有良好的预后。
背景
重症肌无力(MG)是一种自身免疫性疾病,年发病率为每百万人1.7至21.3例。其特点是由自身抗体攻击神经肌肉接头的组分引起的功能性异常,神经肌肉接头是运动轴突和肌纤维之间的高度特异化突触,其中包含对于刺激传递最大效能所必需的特定蛋白复合物。由于其自身的复杂性以及缺乏血液屏障,该结构易受遗传性疾病和免疫攻击的影响。
MG的临床特征是易疲劳和波动性肌无力,最常累及眼肌,可伴或不伴其他肌肉受累。然而,即使在表达相同抗体的患者之间,其临床症状也存在很大差异,使得诊断变得困难。MG最常见的抗体为乙酰胆碱受体(AChR)抗体,但在约50%的眼肌MG患者中以及10%至15%的全身性疾病患者中,AChR抗体的检测结果均为阴性。血清抗体阴性病例通常与肌肉特异性酪氨酸激酶受体抗体或低密度脂蛋白受体相关蛋白抗体有关,但少数病例血清中三种抗体均为阴性(有时称为三重血清阴性MG)。
自身免疫性疾病的起源可能与胸腺异常、免疫调节障碍和激素缺陷有关,这些因素是遗传易感性、微小RNA调控失调、性激素对免疫细胞的影响等先天因素,以及药物和病原体等环境因素共同作用的结果。在胸腺异常的患者中,胸腺瘤与抗AChR MG之间的关系已有研究阐明。虽然自身免疫在胸腺瘤中的作用尚不完全清楚,但已知输出到外周的胸腺细胞可能包括未清除的自身反应性T细胞,这些细胞缺乏对耐受性至关重要的分子成分。
然而,胸腺癌(TC)是一种具有细胞异型性的恶性上皮肿瘤,没有类似胸腺的特征;这也是为什么理论上预计它不会伴随MG的一个原因。 TC是人类最罕见的肿瘤之一(仅占所有胸腺肿瘤的5%),由于其侵入性和转移潜力,TC的侵袭性较强并且预后较差(5年生存率为15-65%)。该肿瘤的组织学特征包括细胞发育不良、细胞异型性、淋巴细胞缺乏和增殖增加、细胞核增大、染色质粗糙、核仁分散以及适量细胞质。
日本的一项大型回顾性分析估计,TC患者中MG的发病率为1%。通常在这种情况下,至少会在癌肿内观察到一些胸腺瘤细胞。然而,作者在一例与局限性TC相关的MG病例中,没有发现胸腺瘤细胞;在胸腺切除术后,临床评估结果良好。本文描述的案例旨在探索和阐明MG和TC之间的关系,并讨论两者之间可能的联系。
材料与方法
患者的信息在签署同意书后获取,来自巴西圣保罗Santa Marcelina医院的神经肌肉疾病门诊部,符合当前伦理标准。组织学材料在圣保罗大学病理学系进行了复查。
病例描述
一名59岁的巴西男性,来自圣保罗,有吸烟和酗酒史,2015年因进行性虚弱无力就医,症状持续5月余。患者表现为疲劳性左侧眼睑下垂、颈部和上肢无力、吞咽困难、呼吸困难以及言语障碍。患者起初在另一家医院就诊,入院检查并对症治疗,临床怀疑MG(重症肌无力),予以泼尼松和吡啶斯的明口服治疗,症状有所改善。后被转诊至Santa Marcelina医院神经医学门诊部,接受了神经肌电图检查,结果显示在低频重复神经刺激下呈现衰减模式。血液检测AChR抗体呈阳性。胸部CT扫描发现前纵隔小肿瘤,直径约为26×14 mm(►图1)。
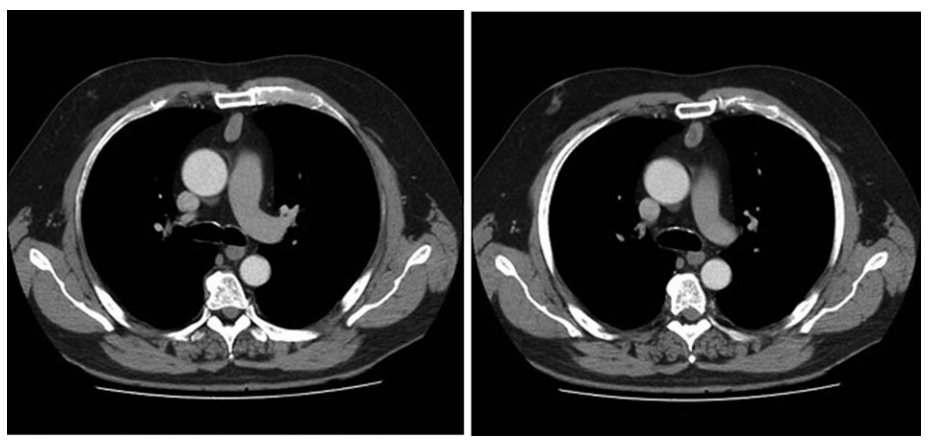
图1. 胸部CT扫描。前纵隔肿瘤,直径26×14 mm,未见明显淋巴结肿大。
随后患者被转诊至胸外科,在症状出现1年后,行胸腔镜胸腺切除术。病理结果显示为胸腺鳞状细胞癌,G1级,小叶生长模式,淋巴细胞外观成熟(►图2)。
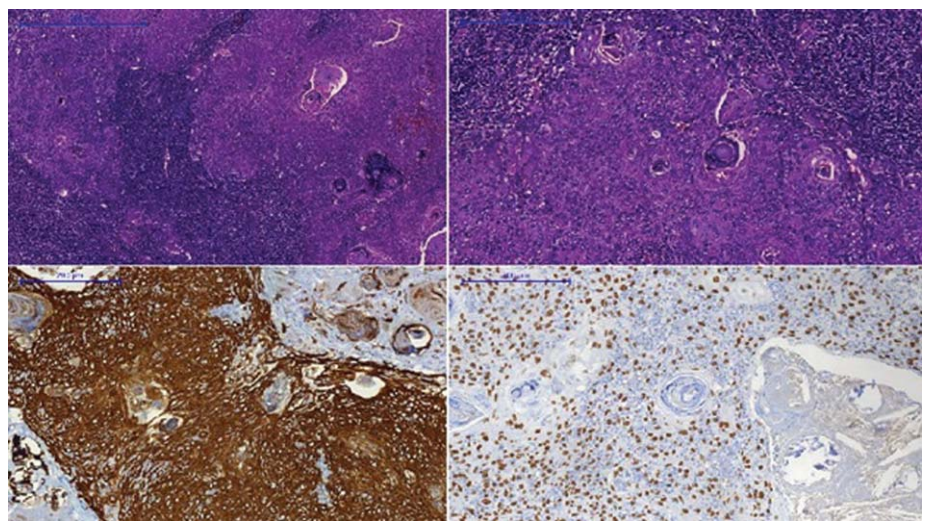
图2. 表皮样角化鳞状细胞癌的组织病理学特征,具有小叶生长模式以及成熟淋巴细胞(HS染色)。
切缘未检测到肿瘤组织。根据Masaoka系统(有包膜肿瘤,显微镜下无包膜浸润)和TNM分级(T1N0M0),该肿瘤属于I期,无淋巴结或血行转移。切除后无肿瘤残留。
自确诊后,患者一直接受口服吡啶斯的明、类固醇和硫唑嘌呤治疗,并持续接受肿瘤学和神经病学团队随访。胸腺切除术后,患者的用药剂量维持了大约1年时间(泼尼松60 mg/天,硫唑嘌呤200 mg/天,吡啶斯的明90mg/天,分4次服用),之后逐渐减少泼尼松剂量,没有症状复发。在最近的门诊复查中,患者服用泼尼松5 mg/天,硫唑嘌呤200 mg/天,吡啶斯的明60 mg/天,分4次服用。日常生活功能保持良好,没有复发或转移的迹象。
评论
重症肌无力(MG)是一种异质性疾病,神经肌肉接头处有多个潜在的的自身抗原靶点,理论上每个靶点都可能导致不同的发病机制。有些MG可能与胸腺病变有关。MG、AChR抗体和胸腺瘤之间的关系已有研究报道,约有10%到20%的MG患者伴有胸腺瘤。大多数其他类型癌症的副肿瘤自身免疫病是由肿瘤细胞中的自身抗原表位触发的,这些抗原表位也存在于靶器官中。一般来说,仅有一小部分癌症病例会并发副肿瘤综合征(通常<5%)。然而,起源于胸腺的肿瘤出现副肿瘤综合征的发生率更高(约50%),可能与其他免疫特征有关。
在健康的胸腺中,AChRs表达于无神经支配的胸腺肌样细胞和胸腺上皮细胞中,这是诱导清除针对AChR的自身反应性T细胞所必需的。然而,并非所有AChR反应性细胞都被清除,其中一些可能包括正常的T细胞储备,由于T细胞能量不足、“免疫忽视”或胸腺外区调节T细胞的调控,T细胞储备处于不活跃状态。MG患者可能会出现耐受性的破坏,主要是由于主要组织相容性复合体II类和辅助分子的异常表达,通过细胞凋亡改变了分子的选择。相反,由于胸腺细胞成熟的肿瘤内微环境异常,MG相关的胸腺瘤可能会产生并输出自身反应性T细胞。此外,此类病例存在自身免疫调节因子表达缺陷,通常会导致外周组织自身抗原(包括胸腺髓质上皮细胞中的AChR α-亚基)的“混杂”表达。
对于胸腺鳞状细胞癌,鉴于该疾病的罕见性以及相关研究数量较少,关于MG出现的理论尚未明确定义。关于该主题的大多数研究是病例描述、病例系列研究以及几种胸腺肿瘤的队列研究,但这些研究并没有直接揭示鳞状细胞癌与MG的关系(►表1)。其可能的致病机制为在胸腺瘤内部发展出TC(胸腺癌),其余的淋巴样细胞负责诱导抗体的产生,方式与纯胸腺瘤类似。当TC起源于胸腺瘤,且在坏死组织中发展时,更常见于B3型胸腺瘤内。
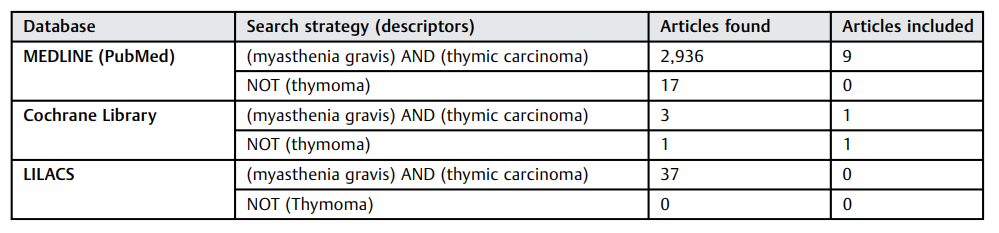
表1. 重症肌无力与胸腺癌关系的数据库检索结果(2019年9月15日)。
然而,在本病例中,并没有任何胸腺瘤成分的证据。作者的数据基本可靠,因为肿瘤很小,并且所有切缘均无肿瘤残留。鳞状细胞癌的肌无力可能有更常见的副肿瘤机制,类似于其他类型的副肿瘤综合征。因此,与胸腺瘤相比,TC患者中MG的发病率较低,可能是由于缺乏胸腺瘤患者中存在的自身免疫促进因素,胸腺瘤副肿瘤综合征的发生率可能高达其他肿瘤的十倍。
部分因素可以影响TC患者的预后:如切除的完全性、Masaoka分期、组织学、肿瘤大小以及淋巴结状况等等。尽管TC具有侵袭性,但该患者具有一些良好的预后因素,并且从肿瘤学和神经病学的角度来看,患者到目前为止恢复良好。其MG症状与其他具有AChR抗体和全身性症状的患者相似。一些作者认为,当TC合并MG时预后较好,这可能与非阴性临床表现提供的早期诊断有关。此外,MG似乎与分化程度更高的肿瘤有关,自身免疫本身可能具有保护作用。然而,该观点尚有争议,也有其他研究表明,伴或不伴肌无力的患者在无复发生存期上没有差异。
除了介绍一种非常罕见的胸腺恶性肿瘤的诊断以及其更为罕见并发症之外,本病例报告还提示TC可能会以不同于胸腺瘤的方式引发抗AChR MG。尽管还需要进一步的研究来获得更有力的证据,但仍然可以推测MG对TC可能有保护作用。
点评
本文报道了一例胸腺鳞状细胞癌(TC)与重症肌无力(MG)并发的罕见案例,并提供了详细的临床资料、治疗过程和随访结果。文章强调了TC与MG可能的关联性,尽管这种关联在文献中鲜有报道。此外,该案例的成功治疗为类似病例提供了宝贵的临床经验,特别是在处理这类复杂疾病时的多学科协作模式。文章中对患者病情的全面评估、清晰的治疗策略描述以及详尽的随访数据,有助于临床医生深入理解该病例。此外,作者还探讨了MG与胸腺瘤及胸腺癌之间的潜在联系,增加了文章的学术价值。
然而,本文也具有一定的局限性。首先,由于是个案报告,其结论的普适性有限,无法直接推广到所有TC伴随MG的病例。其次,文中未提及患者是否接受了其他辅助治疗,如化疗或放疗,这些信息对于完整理解治疗过程也很重要。最后,由于缺乏对照组或更大样本量的研究,仍需要更多研究来验证这一关联性,并探索最佳的治疗策略。总体而言,该篇文章为胸腺癌与重症肌无力之间可能的关系提供了有趣的视角,并为未来的临床研究和实践提供了基础。
本期中文解读
于皓月
/初稿
郑子龙
/初审
范成铭
/校审
范成铭,博士
The Thoracic and Cardiovascular Surgeon 编委
中南大学湘雅二医院
外科学博士,药学博士后,副研究员,博士研究生导师,中南大学湘雅二医院心血管外科主治医师,中华志愿者协会中西医结合专家志愿者委员会心外科专业组常务委员,中国研究型医院学会心脏瓣膜病专业委员会青年委员,湖南省医学会胸心血管外科学专业委员会青年委员,美国阿拉巴马大学伯明翰分校生物医学工程学系国家公派联合培养博士,中南大学十佳大学生、中南大学湘雅二医院青年岗位能手、十佳青年、湖南省卫生健康高层次人才,中南大学“升华学者计划”优秀青年人才。美国胸外科协会(AATS) Evarts A. Graham Memorial Traveling Fellowship 2023年获得者(首位获得该奖项的国内心外科医生,每年仅资助一名心外科医师)。美国Samuel and Jean Frankel心血管中心Fellow。荷兰Catharina医院心胸外科Fellow,比利时Cliniques universitaires Saint-Luc医院心胸血管外科Fellow。主持国家自然科学基金2项、湖南省优秀青年科研基金、湖南省优秀博士后基金各1项,先后获省优秀博士研究生学位论文奖、湖南省医学科技一等奖2项,科技进步二等奖1项,医学十大临床创新技术奖1项。主要研究方向为缺血性心脏病的细胞相关治疗研究,以第一或通讯作者身份在国内外学术期刊发表学术论文30余篇,现担任SCI期刊:Journal of the Renin-Angiotensin-Aldosterone System主编、Clinical and Experimental Hypertension主编,Journal of Cardiothoracic Surgery、BMC Bioinformatics副主编,Clinical Case Reports高级主编,European Journal of Medical Research副主编及心脏病学栏目主编,BioMed Research International、PLoS ONE、PeerJ学术主编,BMC Medicine、Reviews in Cardiovascular Medicine、Thoracic and Cardiovascular Surgeon、BMC Cardiovascular Disorders等多本SCI杂志编委。
The Thoracic and Cardiovascular Surgeon Reports (TCS Reports) 为开放获取期刊,出版与胸部和心血管研究具有重要临床相关性的病例报告,特别强调手术介入措施。TCS Reports 欢迎麻醉、心脏病学、生理学和病理学等胸外科和重症监护领域的投稿。
目标与范围
交流有关心脏、血管和胸部手术治疗的特殊或异常病例
报告胸部、血管和心血管手术中治疗管理的临床新方法
记录可能表明对现有疾病病因与发病机制有的新的或替代性理解的特定临床发现
对发表在母刊The Thoracic and Cardiovascular Surgeon上的研究成果和综述进行补充
促进与胸心血管外科护理相关专业和子专业之间更广泛的信息交流
在TCS Reports上的所有投稿均经过严格的同行盲评。鼓励提交图像和视频等补充资料。
