
#Thieme未来星计划荣誉推出消化病学专题,我们将与未来星计划的小伙伴们持续推荐解读与消化病学相关的最新研究,欢迎关注。同时,欢迎感兴趣的小伙伴加入我们。
本期推荐 & 解读 BY
单飞 | 南昌大学
↓ 消化病学专题丨52
背景
结肠息肉的光学诊断在高流量转诊中心之外的可重复性很差。本研究旨在评估人工智能(AI)辅助的实时光学诊断是否足够准确,以便对微小(≤5毫米)直肠乙状结肠息肉(DRSPs)实施原位切除策略。
在本研究中,采用了一种新型计算机辅助诊断系统(CAD-EYE;富士胶片公司,日本东京),该系统可通过标准内镜检查实时确定息肉特征。本研究的主要目的是前瞻性地评估内镜医师在人工智能辅助下对DRSP的腺瘤组织学检查是否能达到≥90%的NPV。次要研究目的是评估内镜医师单独和人工智能系统单独的光学诊断性能,以及基于光学诊断和组织学的息肉切除术后监测间隔之间的一致性。
Endoscopy
Rondonotti Emanuele et al.
中文内容仅供参考,以英文原文为准,欢迎识别二维码阅读。
方法
连续结肠镜检查的DRSP≥1例患者,在实时人工智能系统(CAD-EYE)的辅助下,由具有不同光学诊断专业知识的内镜医生将DRSP分为腺瘤和非腺瘤。在高置信度人工智能辅助的DRSP光学诊断中,主要终端为腺瘤组织学≥90%负预测值(NPV)(保留和合并有价值的内镜创新[PIVI-1]阈值),以组织病理学为参考标准。根据欧洲胃肠内镜学会(ESGE)和美国多社会工作组(USMSTF)指南计算基于光学和组织学的息肉切除后监测间隔之间的一致性(≥90%;PIVI-2阈值)。
基于卷积神经网络的实时人工智能系统(CAD-EYE)被用于在BLI模式下进行息肉特征描述。简而言之,该人工智能系统通过以下方式提供光学诊断:(i) 在 "位置图 "中识别息肉;(ii) 在内镜图像周围加上彩色括号;(iii) 诊断标记为 "增生性 "或 "肿瘤性"(即腺瘤或非腺瘤,根据制造商的说明)。(图 1)显示了CAD-EYE输出的提供方式。
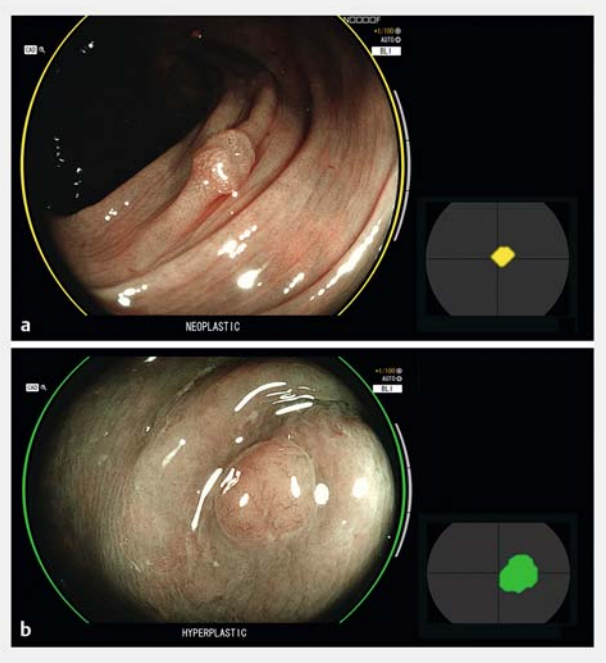
图1. 人工智能系统(CAD-EYE)的输出示意图,显示位置图的颜色编码和内镜图像周围侧边括号的类似颜色:a 黄色点和括号表示腺瘤性息肉(内镜图像下方加上 "肿瘤性 "备注);b 绿色点和括号表示非腺瘤性息肉(内镜图像下方加上 "增生性 "备注)。
内镜医师发现的所有息肉都要报告其大小、位置和形态(根据巴黎分类法)。切除的息肉装在不同的瓶子里,送去进行病理评估。所有小于5毫米的息肉均通过三步顺序过程进行定性(腺瘤或非腺瘤)。息肉光学诊断是在内镜手术过程中通过BLI实时完成的。在第一步(内镜医师单独光学诊断)中,内镜医师在没有人工智能辅助的情况下,使用BASIC分类法将息肉分为腺瘤和非腺瘤。记录内镜医师对光学诊断的置信度(高与低)。内镜医师单独操作的绩效分析只包括高置信度评估的DRSP。在第三步(人工智能辅助光学诊断)中,报告内镜医师综合前两步结果得出的最终诊断结果(腺瘤与非腺瘤)以及置信度(高与低)。只有获得高置信度人工智能辅助光学诊断的DRSP才会被用于计算,与前两个步骤的结果无关。
结果
对389名患者的596个DRSP进行了组织学检索;92.3%的患者通过人工智能辅助高置信度光学诊断。人工智能辅助光学诊断DRSP的NPV(PIVI-1)为91.0%(95 %CI 87.1%-93.9%)。根据ESGE和USMSTF,分别有97.4 %(95 %CI 95.7 %-98.9 %)和92.6 %(95 %CI 90.0 %-95.2 %)的患者达到了PIVI-2临界值。非专家的人工智能辅助光学诊断准确率(82.3 %,95 %CI 76.4 %-87.3%)明显低于专家(91.9 %,95 %CI 88.5 %-94.5%);然而,随着时间的推移,非专家的诊断准确率很快就接近了专家的水平。
从2020年10月到2021年2月,对1134名成人进行了门诊筛查、监测或诊断结肠镜检查。其中,745人被排除在进一步分析之外;因此,389名患者(52.5%男性;平均[SD]年龄:63.7[10.4]岁;)确定了1031个息肉(表1)。在息肉中,30个未被取回(30/1031:2.9%),DRSP占所有息肉的58.6%(604/1031)。
用于AI辅助光学诊断(第三步)的DRSP腺瘤组织学NPV为91.0%(95%CI 87.1%-93.9%),而敏感性、特异性和准确性分别为88.6%(95%CI 83.7%-91.4%)、88.1%(95%CI 83.9%-91.4%)和88.4%(95%CI 85.3%-90.9%)(表2)。单独内镜光学诊断(第一步)和单独AI光学诊断(第二步)的相同数字也详见(表2)。在AI输出可预测和稳定的541个DRSP中,单独内镜师(第一步)和单独AI(第二步)提供的结果在32例(5.9%,95%CI 4.1%-8.2%)中有所不同。
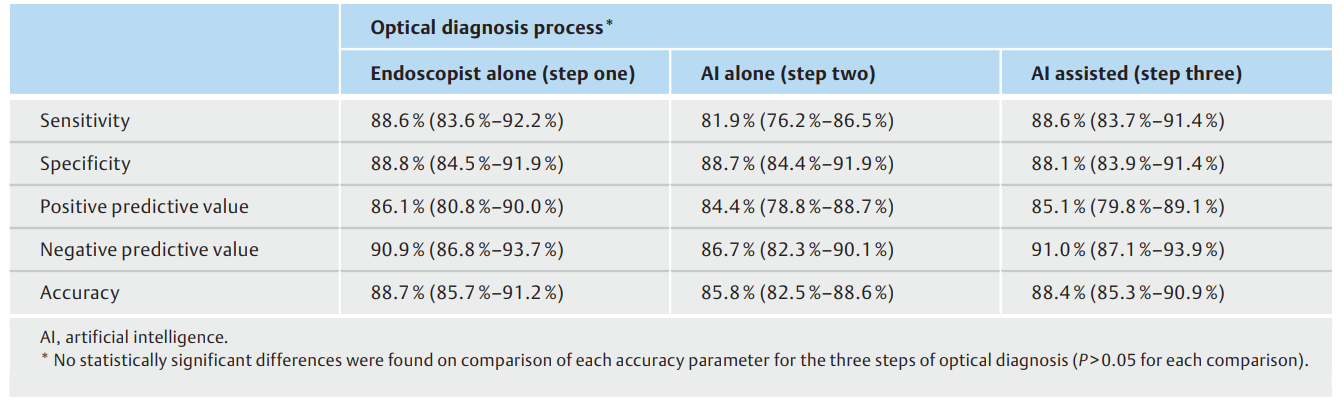
表2. 微小直肠乙状结肠息肉光学诊断过程各步骤的准确度参数(95 %CIs)。
280 名患者(280/389;72.0%,95 %CI 67.2%-76.4%)在结肠镜检查结束时(即只发现微小息肉的患者,所有息肉的评估可信度都很高)可随时获得基于光学诊断的息肉切除术后监测间隔。在ESGE框架内,97.4%的患者(95 %CI 95.7 %-98.9 %)和在USMSTF框架内,92.6% 的患者(95 %CI 90.0 %-95.2 %)(表 3)根据人工智能辅助光学诊断(第三步)正确建议了息肉切除术后的监测间隔。
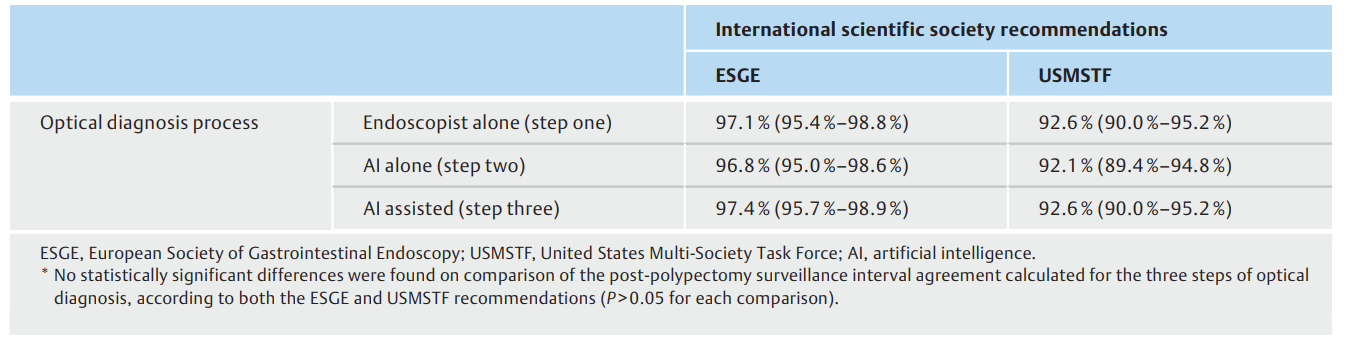
表3. 基于组织学和基于光学诊断的息肉切除术后监测间隔的一致性(95 %CIs)
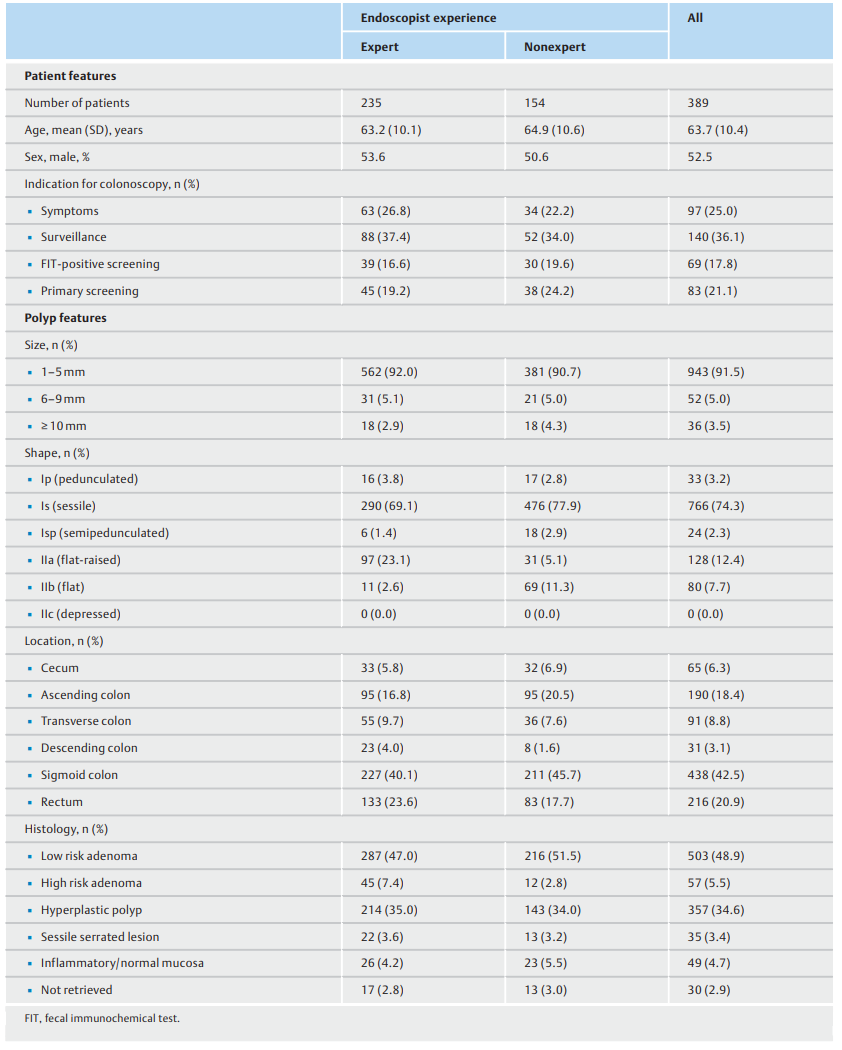
表1. 389 名患者及其息肉的基线特征(根据内镜医生的专业技术划分)。
表4中报告了内镜医师单独(第一步)和人工智能辅助光学诊断(第三步)对专家和非专家的敏感性、特异性、阳性预测值、净现值和准确性的潜在影响。
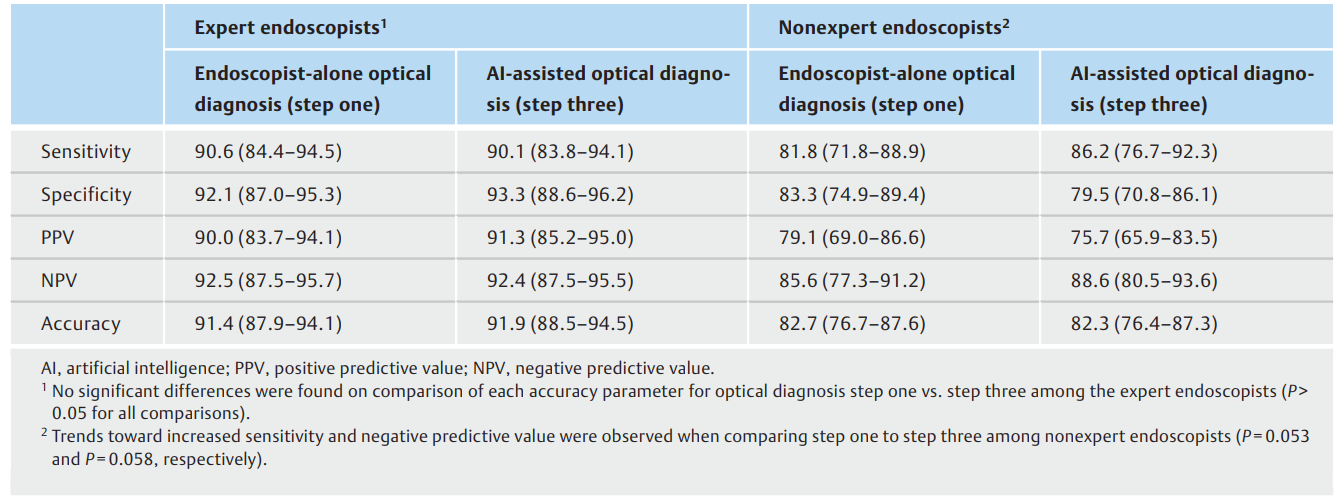
表4. 第一步(内镜医师单独进行光学诊断)和第三步(人工智能辅助光学诊断)对微小直肠乙状结肠息肉进行光学诊断的准确性参数(95 %CIs)和第三步(人工智能辅助光学诊断)光学诊断过程的准确度参数(95 %CIs)。
为了评估潜在的学习曲线,我们根据专业水平,比较了根据前50份DRSP计算出的人工智能辅助光学诊断性能与根据后50份DRSP计算出的人工智能辅助光学诊断性能。就准确率而言,专家与非专业人员之间没有差异(92.0%,95%CI 80.7% - 97.7% vs. 90.0%,95%CI 66.2% - 89.9%),而非专业人员的准确率呈上升趋势(74.0%,95%CI 59.6%-85.3% vs. 88.0%,95%CI 75.6%-95.4%)。有趣的是,非专家评估的最后50个DRSP的AI辅助NPV达到了PIVI-1 临界值(95.2%,95 %CI 76.2 %-99.85%),与专家评估的最后50个DRSP计算出的NPV相似。由非专家评估的一系列连续 DRSP 的准确性趋势见(图 2)。
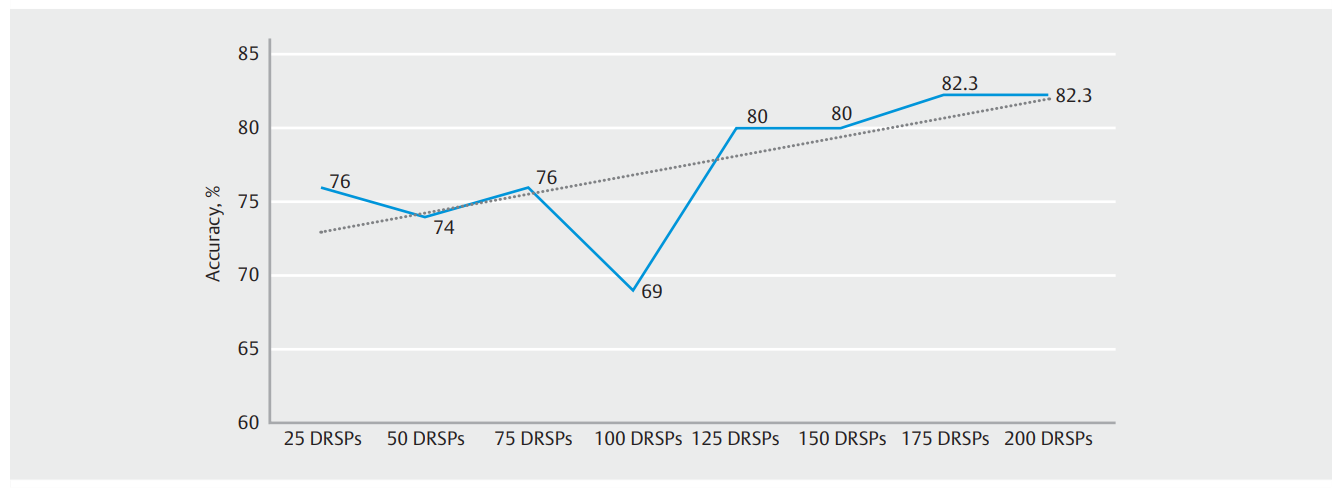
图2. 由非专家评估的一系列连续性微小直肠乙状结肠息肉的准确性趋势(虚线)。DRSP:微小直肠乙状结肠息肉。
结论
人工智能辅助光学诊断符合所需的PIVI临界值。但这并不能抵消内镜医师对高水平信心和专业知识的需求。人工智能系统似乎很有用,尤其是对非专业人员而言。
收获
根据研究,无需光学放大的实时人工智能辅助光学诊断在临床实践中是可行的,可以对90%以上的DRSP进行光学诊断。与内镜医师单独进行的光学诊断相比,人工智能系统在正确诊断方面为专家带来的额外好处似乎微乎其微,但它可能有助于非专家达到将光学诊断纳入临床实践所需的阈值。
欧洲胃肠道内镜学会(ESGE)及其附属学会的官方期刊。
Endoscopy为关于胃肠道内窥镜检查的最新技术和国际发展的重要期刊。在国际编委会的专家指导下,本刊提供高质量的内容,以满足全球内窥镜医师、外科医生、临床医生和研究人员的需求。
Endoscopy每年出版12期,内容包括高质量的综述论文、原创论文、前瞻性研究、有价值的诊断和治疗进展调查、以及对最重要的国内和国际会议进行的深入报道。文章经常辅以在线视频内容。
在Endoscopy上出版的所有论文都经过严格的同行评审。基于在线投稿和快速处理,保证了电子版和印刷版的出版速度。
