
Surgery for Pulmonary Metastases: Long-Term Survival in 281 Patients
Dudek et al.
**中文内容仅供参考,一切以英文原文为准。
背景
在过去几十年里,肺转移瘤切除术(PM)作为治疗转移到肺部的各种肿瘤的综合管理方案的重要部分而被广泛应用。尽管大部分基于单中心回顾性研究的证据不充分,但由于其低围手术期发病率和良好的术后生存率,PM在欧洲进行的所有肺部手术中占比高达15%。迄今为止,还没有随机对照试验明确指出,这些令人满意的结果是由于在高度筛选的患者亚组中更有利的肿瘤病程、施行的系统治疗,还是局部的PM治疗所致。本文的单中心研究旨在评估PM术后结果,并确定影响接受PM治疗的多种原发肿瘤转移患者生存率的因素。这项分析是作者以往研究PM治疗转移性结直肠癌、肉瘤和头颈癌后患者生存的系列研究之一。
方法
作者对在2008年1月至2018年12月间在作者所在三级护理胸科中心接受根治性PM治疗的所有患者进行了回顾性分析。所有患者均符合以下PM选择标准:原发肿瘤部位得到控制、无同步肺外转移(结直肠癌肝转移除外)、肺部病变完全(R0)切除意向和功能上的可手术性。在提供手术之前,所有患者均在多学科肿瘤会议上讨论了治疗方案。对最初不稳定的转移性疾病患者首先进行诱导化疗,随后根据实体瘤的疗效评价标准进行重新评估。肺转移瘤的可切除性通过术前计算机断层扫描(CT)来评估。大多数患者首选可以彻底触诊肺部的保肌侧开胸术。对单个外周转移瘤采用视频辅助胸腔镜手术(VATS)方法进行切除,但这一决定取决于外科医生的偏好。视频辅助小切口开胸术被归类为开放式手术。切除的完整性通过病理检查来确定。患者在第一次PM后3个月和6个月接受CT扫描随访。如果没有复发,则将随访间隔延长至半年,然后再延长至一年。
作者分析了以下变量:性别、PM时的年龄、原发肿瘤部位、原发肿瘤最终治疗完成至PM的时间间隔即肺转移时间(TTLM)、切除的转移性结节的数量、大小和分布、PM的类型和范围、以及对原发肿瘤和/或PM前的辅助治疗。由于不常规进行胸部淋巴结切除或取样,因此无法将淋巴结状态作为预后生存率的评估因素。该研究方案已由机构伦理委员会批准(注册编号425_19 Bc)。该回顾性观察性研究不需要个别患者同意。
术后总生存期(OS)采用Kaplan-Meier方法估计,从第一次PM的日期算起,直到患者死亡或最近一次随访。对于同步转移瘤,双侧分阶段切除术间隔4至6周进行,并将其视为单次转移瘤切除术,分析时使用第一次切除的日期。TTLM计算为原发肿瘤切除或确诊治疗完成至PM日期的间隔。变量通过单因素Cox比例风险模型进行评估,结果以95%置信区间(CI)的风险比(HR)形式给出。连续变量基于接收者操作特征分析获得的截断值进行划分。通过多因素Cox比例风险回归模型评估各种临床病理因素的独立预后意义。p值小于0.05被视为单因素和多因素分析的统计学显著性。用于统计分析的软件是STATISTICA 13.3(StatSoft, 奥克拉荷马州,图尔萨,美国)。
结果
总共281名患者(178例男性)接受了肺转移瘤的根治性切除手术。表1列出了281名患者的临床特征。首次PM时患者的中位年龄为61岁(范围16-84岁)。CRC是最常见的原发病(40.9%,115例),其次是头颈癌(15.7%,44例)和肉瘤(14.3%,40例)。中位TTLM为21个月(范围0-290个月)。53例(18.9%)患者存在与原发肿瘤同步的转移瘤。188例(66.9%)患者的围手术期间隔超过1年,40例(14.2%)患者的围手术期间隔短于1年。
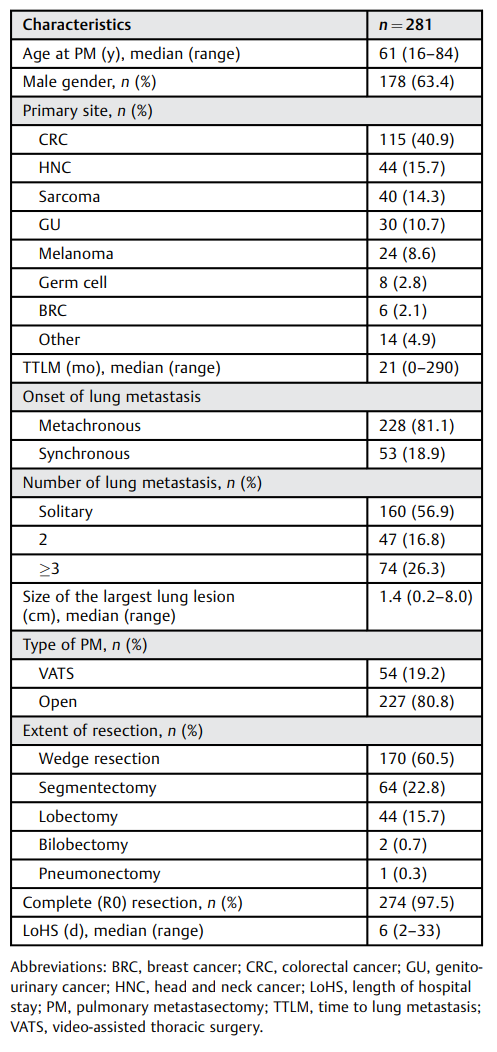
表1. 术前患者特征
手术方法包括保肌侧开胸术(80.8%,227例)和VATS(19.2%,54例)。在首次肺部切除时,大多数患者(60.5%,170例)进行了楔形切除,其次是解剖性肺段切除(22.8%,64例)和肺叶切除(15.7%,44例)。274例(97.5%)患者实现了完全(R0)切除。大多数患者接受了单侧疾病的手术(77.9%,219例)和单个肺转移结节(56.9%,160例)。74例(26.3%)患者有三个或更多的肺转移灶(中位数5个;范围3-23个)。一个患者最多切除的转移性病变数量为23个。
2例(0.7%)由于吸入性肺炎出现围手术期死亡,分别在术后第三天和第四天。23例(8.2%)出现了重大(III/IV级)并发症,包括6例血胸和4例支气管胸膜瘘需再次开胸、4例肺炎、3例切口愈合受损需外科修复、2例脓胸需剥膜、2例术后心房颤动、1例术后膈神经麻痹、以及1例肠系膜缺血需开腹手术。术后住院中位天数为6天(范围2-33天)。
共有166例(60.1%)患者在接受原发病灶切除术后接受了辅助化疗,53例(18.9%)患者在PM前接受了诱导化疗。
在中位随访29个月(范围0-143个月)后,共有134例(47.7%)患者死亡。首次PM后5年OS为47.1%(见图1)。完全(R0)转移瘤切除术后5年的OS率为48.1%,而不完全(R1)切除后的OS率为17.2%。单因素分析显示,66岁或以上的患者(曲线下面积:0.58,HR:1.81,95%CI:1.28-2.56,p=0.0007)生存率较差,而泌尿生殖系统(GU)来源的肺转移瘤(HR:0.45,95% CI:0.23-0.88,p=0.02)与首次PM后更好的生存率相关(见表2)。多因素分析确定GU原发病灶(HR:0.30,95% CI:0.15-0.60,p=0.0008)为独立正相关生存预测指标,而66岁(HR:1.97,95% CI:1.36-2.85,p=0.0003)和不完全(R0)肺部病变切除(HR:3.53,95% CI:1.40-8.91,p=0.0077)为独立负相关生存预测指标(见表3)。性别、TTLM、化疗、转移瘤的数量、大小和分布、手术方法(开放式相比于VATS)和切除范围对长期生存没有显著影响(见表2)。
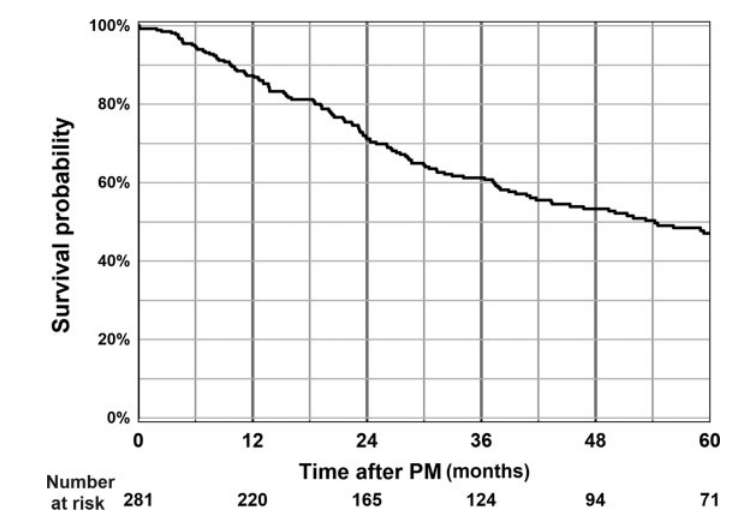
图1. 首次肺转移瘤切除术(PM)后281名患者的总存活率
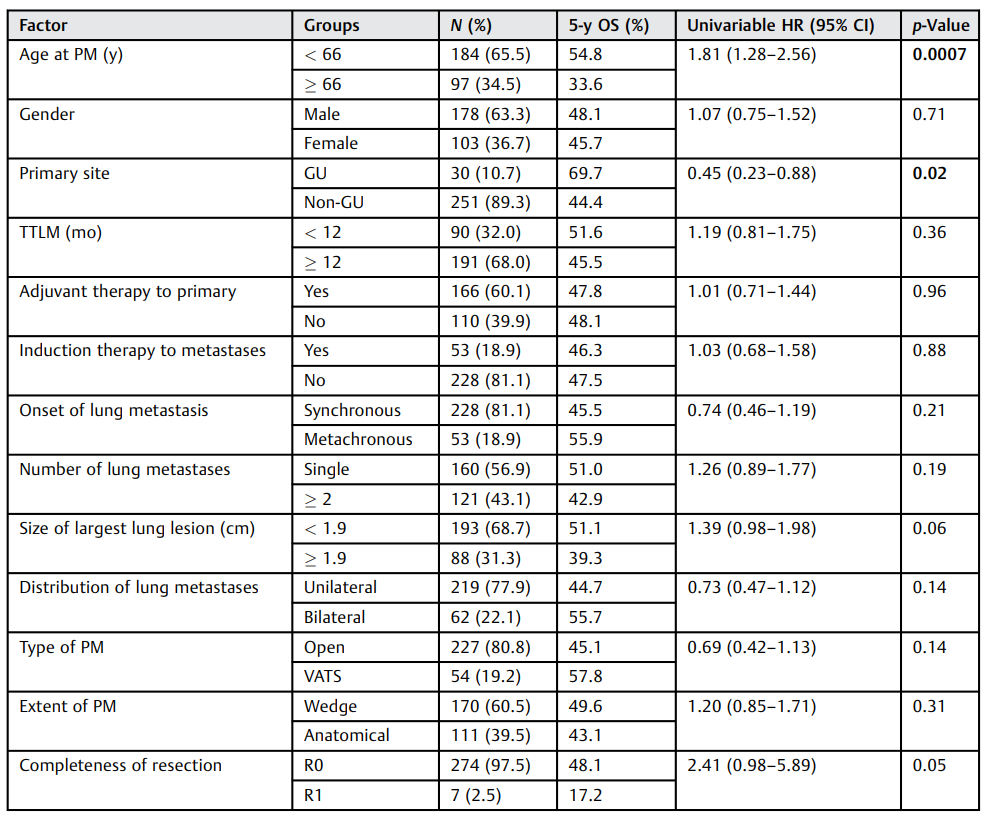
表2. 肺转移瘤切除术后患者生存率影响因素的单因素分析
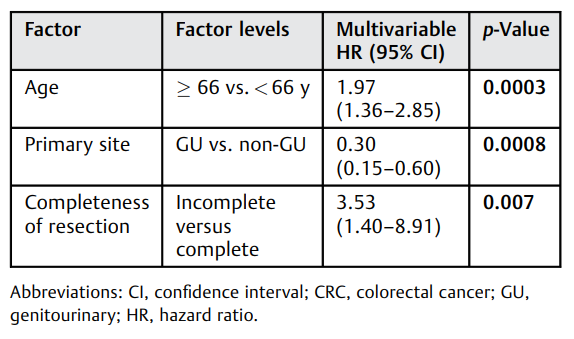
表3. 肺转移瘤切除术后患者生存率影响因素的多因素分析
讨论
所有转移性病变中有20%至54%发现于肺部。使得肺部成为人体第二常见的转移靶器官。自1995年Hellman和Weichselbaum提出介于局限性局部疾病和广泛性癌症之间的少数转移(≤5个转移灶)状态的概念后,人们更加相信PM作为一种局部治疗可以改善患者的生存率。2006年Niibe和Hayakawa把“少数复发”定义为原发肿瘤部位稳定但在一个或多个器官出现一个到几个远处转移/复发。基于少数复发的标准,PM已经成为一种全球标准的根治性局部治疗,适用于特定的心肺功能良好且转移性疾病得到控制的患者。对于非手术候选人,已经提出了放射治疗和消融治疗。对于非手术候选患者,已提出放疗和消融治疗。最近,德国国家健康和护理卓越研究所以及国家综合癌症网络的指南建议在多学科管理转移性结直肠癌和头颈癌的过程中考虑PM。
1997年Pastorino等人发表了涉及18个主要胸外科部门(来自欧洲、美国和加拿大)参与的国际肺转移瘤登记处(成立于1990年)的5,206例肺转移瘤切除术(PM)的结果。这是迄今为止最大的一项多中心回顾性研究,包括了来自各种原发性肿瘤的肺转移病患者。研究认定完全(R0)切除、转移灶数量和长期无病间隔(DFI)是PM后的主要预后因素。完全PM后5年、10年和15年的生存率分别为36%、26%和22%,而不完全切除后的生存率则为5年13%、10年和15年均为7%,强烈支持根治性PM的观点。
Casiraghi等人在一个单机构的10年期间对575名混合原发性肺转移病患者进行的PM治疗的另一项大型回顾性队列研究中,完全切除、生殖细胞组织学类型和DFI 36个月被确认为独立正相关预后因素。该研究甚至确认了更高的PM后生存率,在完全(R0)切除后5年和10年的生存率分别达到46%和29%,而不完全(R1)切除后的生存率为5年和10年均为20%。Cheung等人也在一组243名混合原发性肺转移病患者中,确认了生殖细胞组织学类型和DFI 36个月为PM后的正相关生存预测因素。同步转移、多发转移和不完全切除独立地与较差的OS相关。在本文的研究组中,完全(R0)切除后5年的OS为48.1%,与未能完全切除肺部病变的小亚组(2.5%,7例)中17.2%的5年OS相比更高。在本研究人群中不完全切除被确认为PM后生存的独立负相关预测因素(p = 0.007)。
在本文的研究队列中,生殖细胞组织学类型与PM后更好的OS之间没有关联。8例(2.8%)生殖细胞肺转移患者的5年OS确实比其他组更好(62.7%相比于46.9%),但没有统计学意义(p = 0.49)。这可能是由于生殖细胞组织学类型的患者数量较少。值得注意的是,30例(10.7%)GU肺转移患者的生存率显著高于251例(89.3%)非GU来源患者(5年OS 69.7%相比于44.4%;p = 0.02)(见图2)。基于多因素分析,GU来源的肺转移瘤在队列中是独立正相关生存预测因素。在30例GU转移患者中,有23例(76.6%)为转移性肾细胞癌,3例为膀胱癌,2例为前列腺癌,2例为生殖器癌。Meacci等人报告的转移性肾细胞癌的PM后生存率同样高(5年OS为75%)。作者推测,在其队列中观察到的GU组织学类型相关的突出的OS可能是患者精心选择的结果。
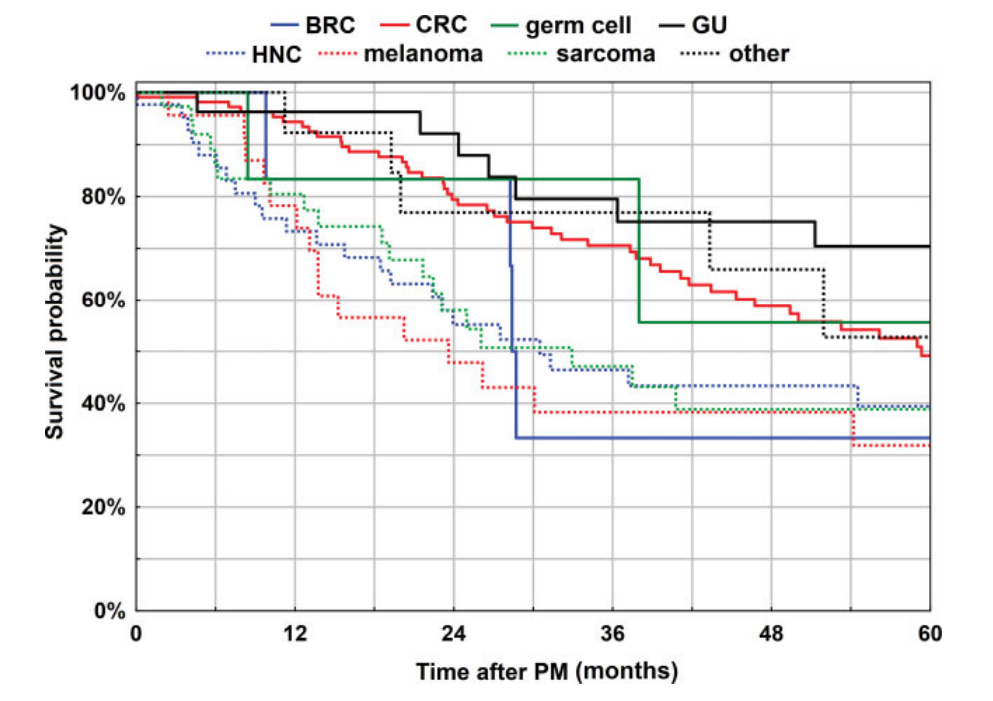
图2. 根据原发部位的首次PM后总体存活率
有趣的是,本文的单因素Cox比例风险模型分析显示,66岁及以上的患者与年轻患者相比,生存率显著更差(5年OS 33.6%相比于54.8%,p=0.0007)。患者在接受PM时的年龄被识别为多因素分析中的独立预后因素。然而,考虑到可接受的生存率,作者建议对可以完全切除转移病变的心肺功能良好的老年患者实施根治性PM。Barone等人得出了类似的结论,他们报告了老年患者群体在完全(R0)切除CRC后更不利的21.2%的5年OS。
与许多作者不同,本文作者在研究组中没有发现肺转移的发生时间(同步相比于异步)或肺转移时间(12个月相比于少于12个月)与预后之间的显著关系。作者更喜欢使用“TTLM”而不是“DFI”,因为作者不认为发展转移性疾病的患者是“无疾病状态”。肺部病灶的数量、大小和分布在队列中没有预后意义。
本文研究有几个局限性:(1)单中心回顾性设计;(2)术后结果和生存率是在高度筛选用于根治性手术的患者中评估的;(3)不同原发肿瘤组织学类型可能影响了整个组的OS;(4)由于缺乏标准,无法评估纵隔/肺门淋巴结切除的预后影响;(5)没有非手术管理的对照组进行比较。考虑到评估PM与非手术治疗转移性结直肠癌是否真正提供生存优势的结直肠癌肺转移瘤多中心随机试验存在患者招募困难(93例),该研究提前终止,作者推定了一项设计良好的大型多中心队列研究,包括对照组和更长的随访期,也可能有效评估PM对特定类型转移性癌症的价值。
结论
本文的10年的单中心经验表明,PM与长期生存利益相关。在筛选肺转移瘤切除术的多学科患者时,应考虑患者年龄、原发肿瘤组织学类型和完全切除的可行性。
点评
尽管证据不足,但肺转移瘤切除术(PM)被广泛用于改善患者的存活率。本文的单机构分析旨在评估PM术后结果,并确定影响接受PM治疗的多种原发肿瘤转移患者生存率的因素。作者对2008-2018年间所有接受根治性PM的患者进行了回顾性分析,并使用单因素和多因素Cox比例风险模型评估与原发肿瘤、转移和相关治疗有关的因素对总体生存(OS)的影响。连续变量的截断值通过接收者操作特征分析来确定。在本研究中,281名患者(男性178名,中位年龄61岁)接受了PM。围手术期发生了2例(0.7%)死亡和23例(8.2%)重大并发症。原发肿瘤治疗与PM之间的中位间隔为21个月。最大转移瘤的中位大小为1.4厘米。经过中位随访29个月后,134名患者(47.7%)已经死亡。首次PM后5年的总生存率(OS)为47.1%。在274名(97.5%)患者中实现了完全切除。围手术期发生了2例(0.7%)死亡和23例(8.2%)重大并发症。原发肿瘤治疗与PM之间的中位间隔为21个月。最大转移瘤的中位大小为1.4厘米。经过中位随访29个月后,134名患者(47.7%)已经死亡。首次PM后5年的总生存率(OS)为47.1%。在274名(97.5%)患者中实现了完全切除。多变量分析确定泌尿生殖系统起源(HR:0.30,95%CI:0.15-0.60,p=0.0008)为独立正相关生存预后指标;不完全切除(HR:3.53,95% CI:1.40–8.91,p=0.0077)和PM时年龄为66岁(HR:1.97,95% CI:1.36–2.85,p = 0.0003)是负相关预后指标。将PM作为多模式治疗的一部分,在选定的人群中是合理的,本文确定了年龄、原发肿瘤起源和切除的完整性作为独立的生存预后指标。
本期中文解读
冷奇濠
/初稿
李逸尘
/初审
范成铭
/校审
范成铭,博士
The Thoracic and Cardiovascular Surgeon 编委
中南大学湘雅二医院
范成铭博士的研究方向是心血管外科、缺血性心脏病的干细胞治疗。他主持了国家自然科学基金青年项目、湖南省自然科学基金优秀青年项目等多项课题。已在国际期刊发表学术论文55篇。他还是美国心脏协会AHA成员、动脉硬化、血栓形成和血管生理学委员会成员、国际动脉粥样硬化学会会员。
德国胸心血管外科学会会刊。
The Thoracic and Cardiovascular Surgeon 发表来自国际公认的胸心血管外科医师、心脏病学家、麻醉学家、生理学家和病理学家的最高标准文章。本刊是这一领域工作者的重要资源。
原创论文、简讯、综述和重要会议公告将报告关键的临床进展,同时为读者提供心血管和胸外科的理论背景。病例报告在我们的开放获取姊妹期刊The Thoracic and Cardiovascular Surgeon Reports上发表。
