
#Thieme未来星计划荣誉推出消化病学专题,我们将与未来星计划的小伙伴们持续推荐解读与消化病学相关的最新研究,欢迎关注。同时,欢迎感兴趣的小伙伴加入我们。
本期推荐 & 解读 BY
单飞 | 南昌大学
↓ 消化病学专题丨20
当内脏器官的灌注不能满足正常的代谢需求时,就会发生肠系膜缺血,随后导致腹部症状,如弥漫性餐后疼痛、腹膜炎、食物恐惧和体重减轻。肠系膜缺血通常分为急性和慢性表现,但由于与其他腹部病变的症状有显著重叠,因此在初次就诊时常被误诊。及时识别和诊断、肠系膜血运重建和重症监护治疗仍然是患者获得最佳结局的主要治疗手段。本综述将重点介绍急性肠系膜缺血与慢性肠系膜缺血、病因、诊断标准、治疗方案,并将强调胃肠道和血管外科医生在及时处理这种疾病以预防极差预后方面的共同作用。
Clinics in Colon and Rectal Surgery
Audu et al.
中文内容仅供参考,以英文原文为准,欢迎识别二维码阅读。
内脏血流的解剖学和生理学
供应腹部内脏器官的三条主要内脏动脉是腹腔动脉(CA)、肠系膜上动脉(SMA)和肠系膜下动脉(IMA)。无论病因如何,长期缺血都会导致肠粘膜屏障的破坏,主要是通过活性氧代谢物和中性粒细胞的作用。在缺血期间,肠道屏障完整性受损,并允许细菌通过粘膜易位并进入周围的淋巴结和组织。 随着有氧代谢减慢和三磷酸腺苷(ATP)被消耗,线粒体膜的完整性受到损害。如果缺血持续超过45分钟,则细胞死亡。
急性肠系膜缺血
急性动脉肠系膜缺血的诊断和治疗具有挑战性,死亡率高。虽然每1000例住院患者中只有不到1例,但在需要血运重建的患者中,住院死亡率仍保持在17%至21%左右。AMI对女性的影响是男性的三倍,通常见于患有多种合并症的老年患者。
病因
AMI的临床危险因素包括心房颤动/扑动病史、近期心肌梗死、充血性心力衰竭、心内膜炎、肠系膜静脉血栓形成或外周动脉栓塞。主动脉夹层或自发夹层的内脏动脉夹层也可引起AMI。最后,患者可以在内脏血管未闭的情况下从全身性“低流量状态”发展为肠系膜缺血。
动脉栓塞是AMI的最常见原因,通常约占病例的40%至50%。在计算机断层扫描血管造影(CTA)或磁共振血管造影(MRA)上看到的栓塞性闭塞的血管造影标志是刚好超出结肠中动脉起点的突然切断(图1)。
动脉血栓形成是AMI的第二大常见病因,见于20%至35%的病例。肠系膜动脉血管痉挛通常继发于大剂量血管加压药。它通常分布在SMA中,是AMI的一种形式,约占20%。
门静脉和肠系膜静脉血栓形成可因流出道梗阻导致灌注不足而损害内脏灌注。这占肠系膜缺血的5%至10%,死亡率为19%至23%。
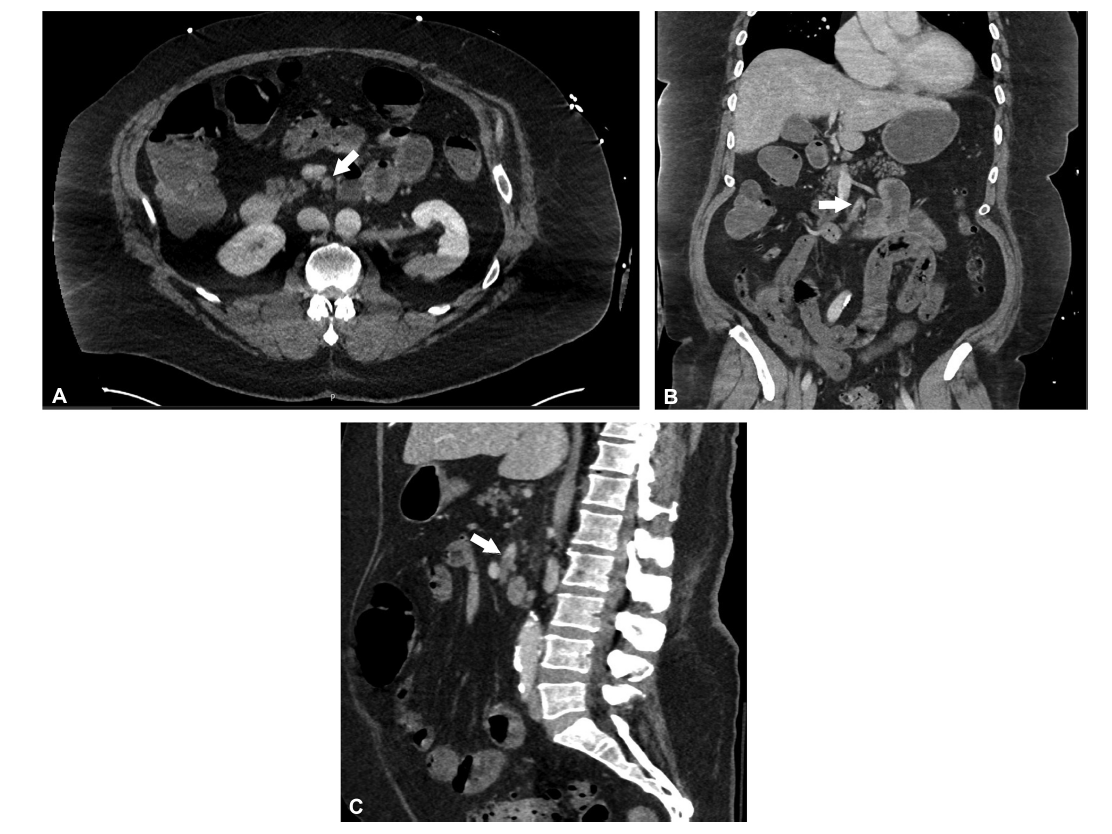
图1. 急性肠系膜缺血。白色箭头表示该患者的(A)轴向、(B)冠状和(C)矢状位中肠系膜上动脉(SMA)的动脉血流减少和栓塞区域。在这种情况下,血栓位于结肠中动脉分支的远端,并通过栓塞切除术进行治疗。
诊断
实验室检查:白细胞增多、酸中毒和乳酸升高。AMI诊断主要依靠影像学检查。诊断性动脉造影为金标准。CTA是评估肠道和血流的最佳方式。因为CTA的敏感性和特异性分别为93%和96%。
治疗
AMI的主要治疗方法是血运重建、肠道评估(必要时可进行切除)和术后重症监护。应首先开始抗凝治疗、广谱抗生素和液体复苏以支持肠系膜灌注。
开放修复术通常涉及使用Fogarty球囊导管直接插入SMA的栓子切除术,但如果解剖结构合适,髂骨到SMA和主动脉到SMA旁路也是可行的。随着血管内技术的进步,也可以采用混合方法——通常需要取栓术,然后逆行支架置入近端SMA和主动脉。
慢性肠系膜缺血
CMI,有时被称为肠绞痛,餐后疼痛为典型症状,导致进食减少和体重减轻。当初级和侧支循环不足以提供为分泌和吸收的代谢过程提供氧气以及增加蠕动活动所需的餐后充血反应时,CMI 患者就会出现症状。
病因学
CMI 最常见的病因是动脉粥样硬化性疾病引起的动脉阻塞,约占90%的病例。动脉粥样硬化性病变通常发展为斑块从主动脉延伸而来,因此,大多数位于肠系膜动脉的起点,可以延伸到分支2至3厘米(图2)。CMI的非动脉粥样硬化病因很少见,包括血管炎、系统性狼疮、血栓闭塞性血管炎、自发性夹层、纤维肌发育不良、神经纤维瘤病、放射性动脉炎、主动脉缩窄、肠系膜静脉狭窄和可卡因使用引起的药物性动脉病。
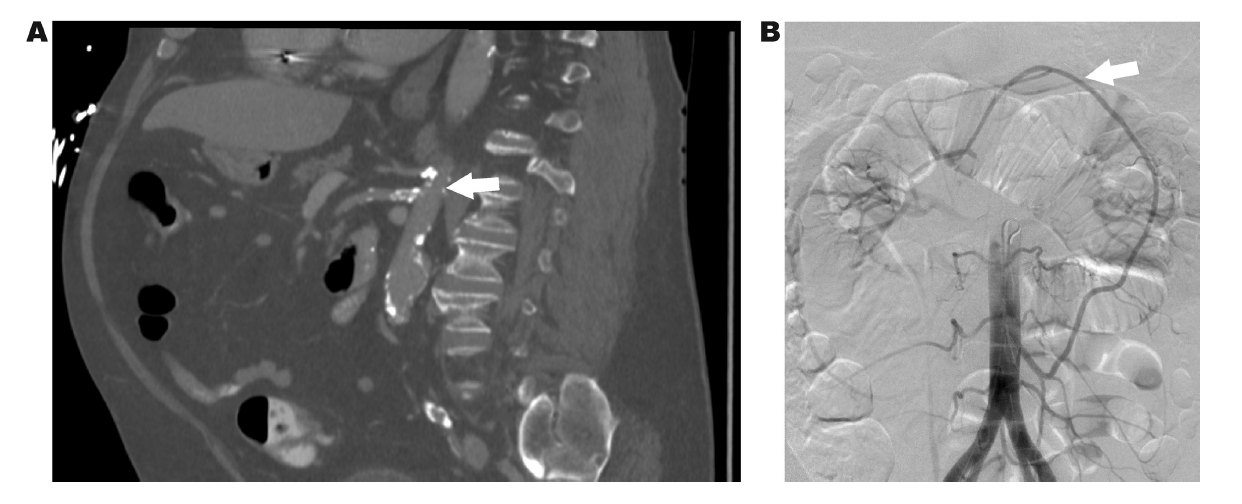
图2. 慢性肠系膜缺血。(A)白色箭头指向轴向视图中肠系膜上动脉(SMA)和腹腔动脉起点处由于严重动脉粥样硬化和钙化引起的狭窄区域。(B)在慢性肠系膜缺血的情况下,通过Riolan弧(白色箭头)从SMA到肠系膜下动脉(IMA)的发达侧支发育良好。
诊断
CMI的诊断通常是滞后的。大多数情况下,肠系膜动脉狭窄的发现是在横断面影像学上发现的。我们主张将CMI纳入所有慢性腹痛患者的鉴别诊断。对于疑似CMI的患者,有几种评估方法。这些检查包括肠系膜多普勒超声、CTA、MRA 和造影剂血管造影。
治疗
CMI患者的治疗目标是缓解腹部症状、促进体重增加和防止AMI。血管外科学会(Society for Vascular Surgery,SVS)实践指南建议,所有有体重减轻、腹泻或餐后疼痛症状的CMI患者均应进行血运重建。通过一期支架置入术进行血管内入路是超过80%且病变合适的CMI 患者的首选。开放性血运重建的选择包括顺行旁路术(主动脉流入术)、逆行旁路术(髂骨流入术)或主动脉内脏动脉内膜切除术。使用混合手术治疗,这涉及SMA暴露,将支架逆行放置到主动脉中,以及初级SMA修复术或补片血管成形术。通常被称为逆行肠系膜支架置入术(ROMS)。
结论
肠系膜缺血可导致肠坏死、多系统器官衰竭和死亡。及时诊断和血运重建仍然是这些患者的主要治疗手段。对于肠道完整性可能受损的患者,应根据需要进行肠道检查和切除。
讨论
肠系膜缺血应及早诊断,及早治疗,治疗方法包括支持疗法和手术治疗。肠系膜上动脉栓塞可行取栓术,血栓形成则可行血栓内膜切除或肠系膜上动脉-腹主动脉“搭桥”手术,如果已有肠坏死,应作肠切除术。肠系膜上静脉血栓形成需施行肠切除术,切除范围应包括全部有静脉血栓形成的肠系膜,否则术后静脉血栓有继续发展的可能,术后应继续行抗凝治疗。
Clinics in Colon and Rectal Surgery 为综述类期刊,出版有关小肠、结肠、直肠和肛门疾病的专题。
本刊专门面向涉及肠道疾病的临床医生、研究人员和教育工作者,广泛涵盖了基础信息、有争议的临床问题以及成熟和创新性诊断技术。
期刊主题全面覆盖整个专业,可作为 3 - 4 年的教育课程和认证考试的学习材料。所包含的研究和临床资料还能够使医生随时了解该专业的最新进展。
