
#Thieme未来星计划荣誉推出有机化学专题,我们将与未来星计划的小伙伴们持续推荐解读相关的论文与研究,欢迎关注。同时,欢迎感兴趣的小伙伴加入我们。
本期推荐 & 解读 BY
不闻 | 南京大学
↓ 有机化学专题丨12

Jiwei Wu, Kejun Jin, Ruiyou Wang, Xingyu Wang, Xiaoxiao Yu, Liangcheng Zhong, Jianguo Liu
Synthesis
DOI: 10.1055/a-1942-7110
总结与评述
本文主要讲述在无金属和无外部氧化剂条件下,建立了分子内C(sp3)-H /C(sp3)-H交叉偶联的电化学方法。此方法提供了一种简单而有效的途径,以中等到较高的收率构建了具有生物活性的4-喹诺酮骨架。
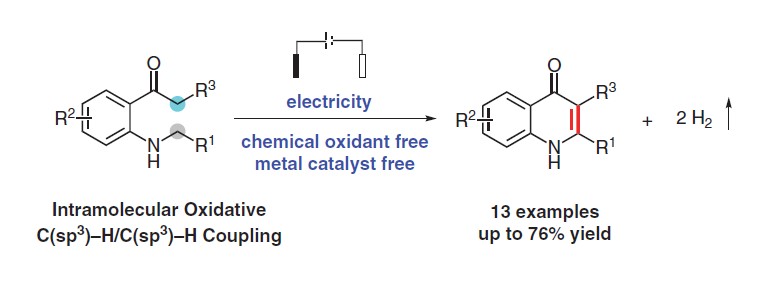
图1|电催化分子内C(sp3)-H /C(sp3)-H交叉偶联
背景介绍
由于Aza-heterocycles广泛存在于各种的生物活性分子之中,经常被应用于治疗领域。在众多杂环杂环化合物中,4-喹诺酮类化合物是生物活性分子和天然产物中最常见的骨架。此外,许多4-喹诺酮衍生物表现出各种药理活性,并已在日常生活中使用,如被用作抗菌药物:恶唑酸、奥唑沙星和环丙沙星,被用于治疗HIV感染、兽药和囊性纤维化的药物:伊维格雷韦、马博沙星和艾瓦克特(Figure 1)。
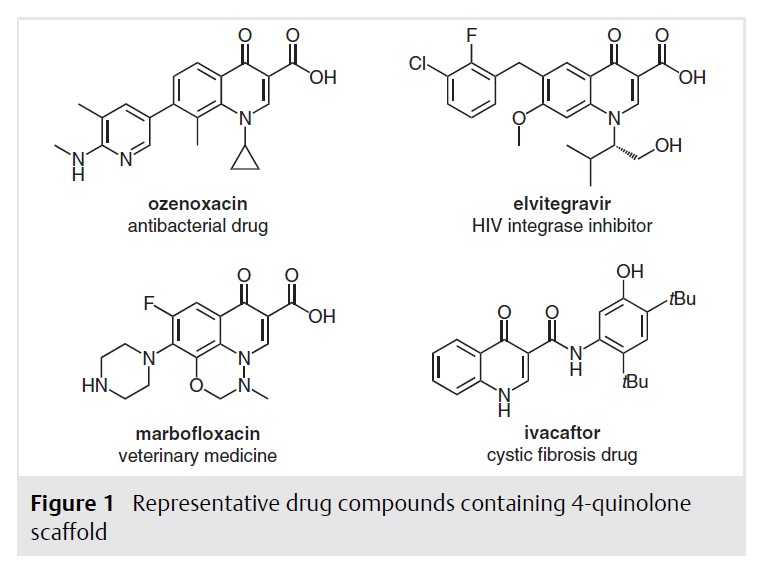
图 2|众多含4-喹诺酮骨架的药物分子
到目前为止,已经开发了多种方法来构建4-喹诺酮骨架,如Niementowski反应,conradl-limpach反应, Camps环化,钯催化羰基化,钌催化还原反应,钛介导的还原偶联反应,铜催化环化反应等。然而,高温(高达300℃),强碱或酸和使用的金属使其对大规模应用是危险的。近年来,Long的课题组和Huang的课题组利用TEMPO作为氧化剂,开发了一种无过渡金属氧化环化反应,合成4-喹诺酮类化合物(Scheme 1a)。尽管取得了进展,但使用的过量氧化剂不符合绿色化学发展要求。如今,有机电化学合成已发展成为一种高效的化学键构建方法,因为这种合成策略利用电子作为清洁的反应物,规避使用化学计量的化学氧化剂。
这里作者揭示了一种高效的电化学方法,首次实现在无金属和无外部氧化剂条件下,通过分子内C(sp3)-H/C(sp3)-H交叉偶联合成4-喹诺酮类化合物(Scheme 1b)。
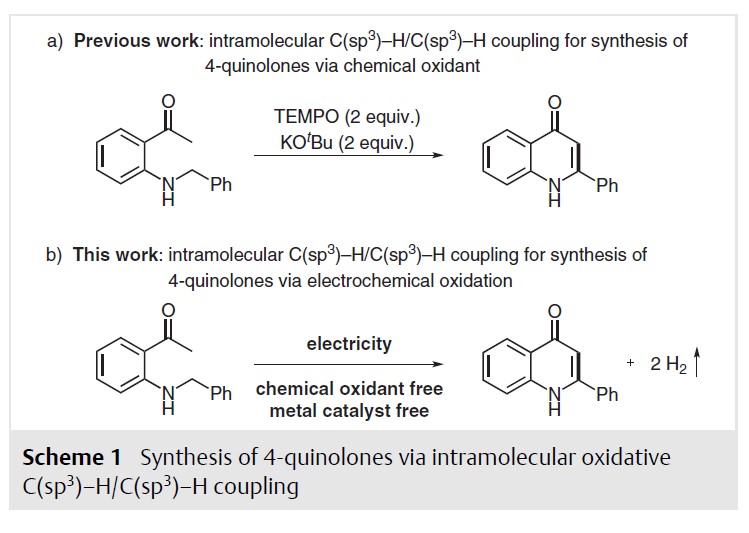
图3|化学氧化和电氧化合成4-喹诺酮类衍生物
条件优化与底物拓展
首先,作者使用N-苄基-2-氨基苯乙酮(1a)作为模板底物开始对该反应进行研究。令人高兴的是,在60℃的条件下,以铂为阳极和阴极,NaOtBu为碱,nBu4NBF4为电解质,DMSO和tBuOH为混合溶剂,10 mA恒流3小时,得到了73%的预期产物2-苯基喹啉-4(1H)-1 (2a)。

图4|条件优化
在确定最佳反应条件后,作者探索了这种电化学分子内氧化偶联方案的适用范围(Scheme 2)。特别需要注意的是,R1为脂肪族取代基如环己基和苄基在该方案中不能被兼容(Scheme 2,2n,2o)。
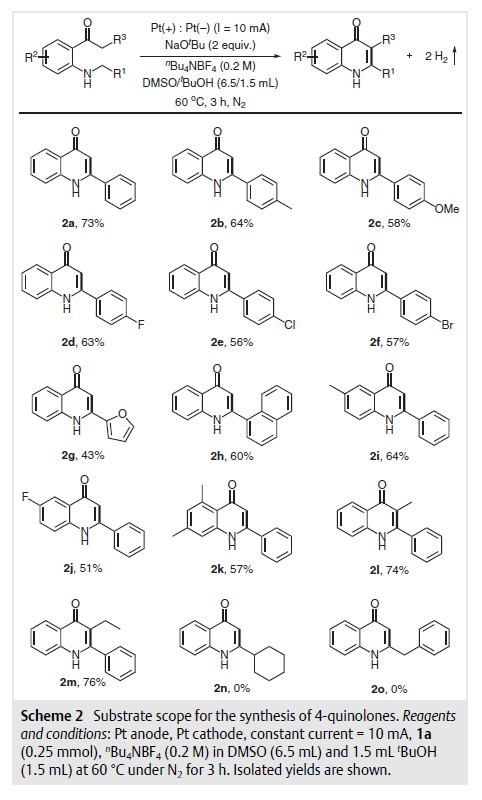
图5|底物拓展
机理研究
为了确定合理的机制,在标准反应条件下以1-(2-(亚苄基氨基)-苯基)-1-乙酮和2-苯基-2,3-二氢喹啉-4(1H)-酮为底物,得率分别为57%和52%( (Scheme 3, I and II),然后在标准条件下以Nmethylated底物1p为底物,仅能从GC-MS中检测到痕量产物2p。
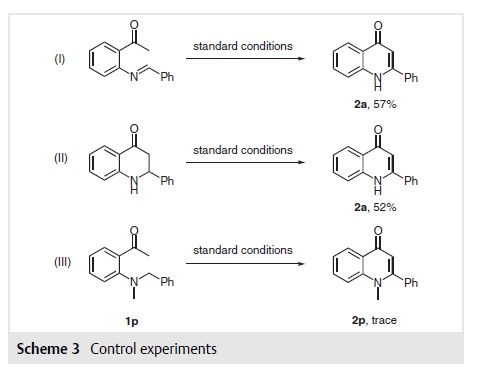
图6|控制实验
根据文献报道以及以上实验结果,作者提出了一种可能的机制,如Scheme 4所示。首先,1a在阳极被氧化,通过单电子转移过程生成自由基阳离子A;随后,自由基阳离子A被NaOtBu攫取氮上质子后转化为亚胺B,在NaOtBu存在下形成中间产物C;烯醇互变异构后形成烯醇D与分子内亚胺发生亲核加成反应,形成环状产物E,中间产物E被阳极进一步氧化,生成喹诺酮类产物2a。叔丁醇在阴极被还原,析出氢气。
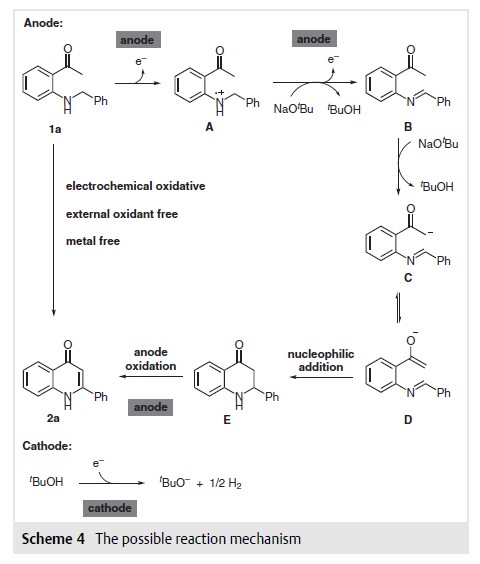
图7|机理循环
总结与评述
综上所述,作者开发了一种温和、绿色的电化学分子内氧化C(sp3)-H /C(sp3)-H偶联的方法,为构建4-喹诺酮类药物提供了一条直接有效的途径。
