
#Thieme未来星计划荣誉推出消化病学专题,我们将与未来星计划的小伙伴们持续推荐解读与消化病学相关的最新研究,欢迎关注。同时,欢迎感兴趣的小伙伴加入我们。
本期推荐 & 解读 BY
单飞 | 南昌大学
↓ 消化病学专题丨35
背景:T1结直肠癌(CRC)的发病率随着CRC筛查项目的实施而增加,目前尚不清楚基于非筛查检测患者的T1 CRC的转归和风险模型能否外推到筛查检测的T1 CRC。本研究旨在比较筛查项目内外T1 CRC患者的分期分布和肿瘤学转归。
方法:收集荷兰12家医院2014年至2017年间确诊的T1 CRC患者的数据。使用多变量logistic回归比较筛查检测和非筛查检测患者在诊断时是否存在淋巴结转移(LNM)。Cox比例风险回归用于分析复发时间(TTR)、无转移生存期(MFS)、癌症特异性生存期(CSS)和总生存期的差异。此外,评估各组LNM常规风险因素。
结果:共纳入1803例患者(筛查检出1114例[62%]),中位随访51个月(四分位数范围30)。筛查检出和未筛查检出患者的LNM比例无显著差异(12.6%vs 8.9%;优势比1.41;95%CI 0.89-2.23);LNM预测模型在两组中表现相同。筛查计划内外患者的3年和5年TTR、MFS和CSS相似。然而,筛查检出的T1 CRC患者的总生存期明显更长(调整后的风险比0.51;95%CI 0.38-0.68)。
结论:筛查检测和未筛查检测的T1 CRC具有相似的分期分布和肿瘤学结局,因此可以同等对待。然而,筛查检测的T1 CRC患者表现出较低的非CRC相关死亡率,导致较长的总生存期。
Endoscopy
Oncologic outcomes of screen-detected and non-screen-detected T1 colorectal cancers
van der Schee Lisa et al.
中文内容仅供参考,以英文原文为准,欢迎识别二维码阅读。
介绍
基于人群的结直肠癌(CRC)筛查检测到的CRC可以分期,其特征是与未筛查检测到的CRC相比,I期的比例更高,IV期的比例更低。这种分期分布是否也在筛查检测到的黏膜下侵袭性(T1)CRC中存在尚不清楚。鉴于对于T1 CRC使用保留器官的治疗策略,确定筛查检测到的T1 CRC中转移和肿瘤结局的预测因子是否与未筛查检测到的病例中的预测因子具有可比性至关重要。特别是因为迄今为止使用的大多数风险预测模型都是基于来自预筛查期未筛查到的T1 CRC的数据。
本研究的目的是评估筛查检测和未筛查检测的T1 CRC患者的分期分布和肿瘤学结局,并研究用于指导临床决策的既定LNM风险因素是否可以外推到T1 CRC患者的筛查人群中。
方法
研究设计和患者选择
进行了一项多中心回顾性观察队列研究。通过荷兰癌症登记处确定了2014年至2017年间来自12家医院(包括一家学术医院)的所有连续确诊为T1 CRC的患者。荷兰国家筛查计划于2014年开始,按年龄组逐步引入。55-75岁的男性和女性每2年随访一次,采集粪便样本,用于使用粪便免疫化学测试(FIT)检测潜血。在我们的研究期间,随访率为2014年目标人群的40%,2017年上升到95%。
结肠镜检查的原因(即基于人群的CRC筛查计划或其他原因)从个人电子病历中检索,这些病历在参与医院进行了审查。当地病理学报告确认pT1 CRC的诊断时,患者被纳入。排除标准是:(i)CRC的遗传倾向(Lynch或家族性腺瘤息肉病综合征);(ii)炎症性肠病;(iii)诊断时的同步CRC或以前的CRC≤T1 CRC诊断前5年;(iv)非腺癌;(v)缺少病理学或内镜报告;和(vi)新辅助(化学)放疗。
决定因素和终点
主要结果是LNM的比例。定义为诊断时手术切除标本中的肿瘤阳性淋巴结。此外,我们研究了LNM的常规临床和组织病理学危险因素在筛查检测和非筛查检测患者中的表现是否相似。
数据分析
使用分类变量的卡方检验和连续数据的Mann-Whitney U检验比较筛查检测和未筛查检测的T1 CRC患者的基线特征。类别数据表示为带有百分比的频率,连续数据表示为具有相应四分位数范围(IQR)的中位数。用单变量和多变量logistic回归分析了接受手术治疗的患者组(包括原发性和完全性手术)的适应症(筛查检测或非筛查检测)与LNM之间的潜在关联。在多变量模型中,我们调整了年龄、性别、息肉位置、息肉形态、息肉大小、分化程度、淋巴血管浸润(LVI)以及手术期间取回的淋巴结数量。
结果
在参与的医院中,共有2258名T1 CRC患者被确定,其中455名因符合一项或多项排除标准而被排除在外(图1)。
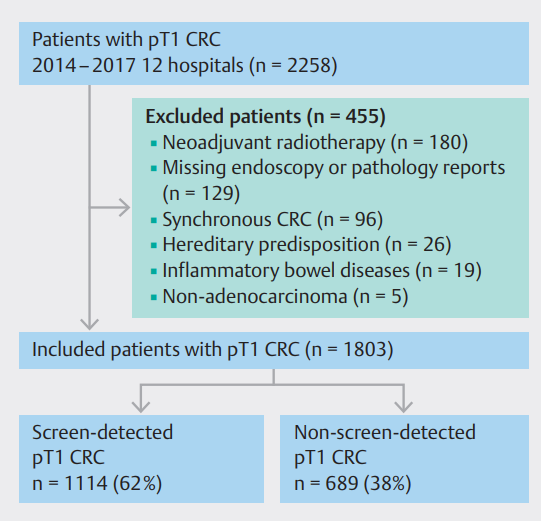
图1. 纳入T1结直肠癌(CRC)患者的流程图。
虽然两组之间的整体手术切除率相当(筛查检测组和非筛查检测组分别为52.5%和53.8%),但在非筛查检测组患者中更经常进行初级手术(26.8%vs.34.4%;P<0.001)。在首先接受内镜切除治疗的1268名患者中,397/816例筛查检测的T1 CRCs(48.7%)表现出一种或多种组织病理学高危特征,相比之下,223/452例非筛查检测的T1 CRCs(49.3%;P=0.97)。这些内镜切除高危T1 CRCs患者的治疗策略(完成手术或监测)在筛查检测和非筛查检测患者之间没有显著差异(P=0.09)(图2)。
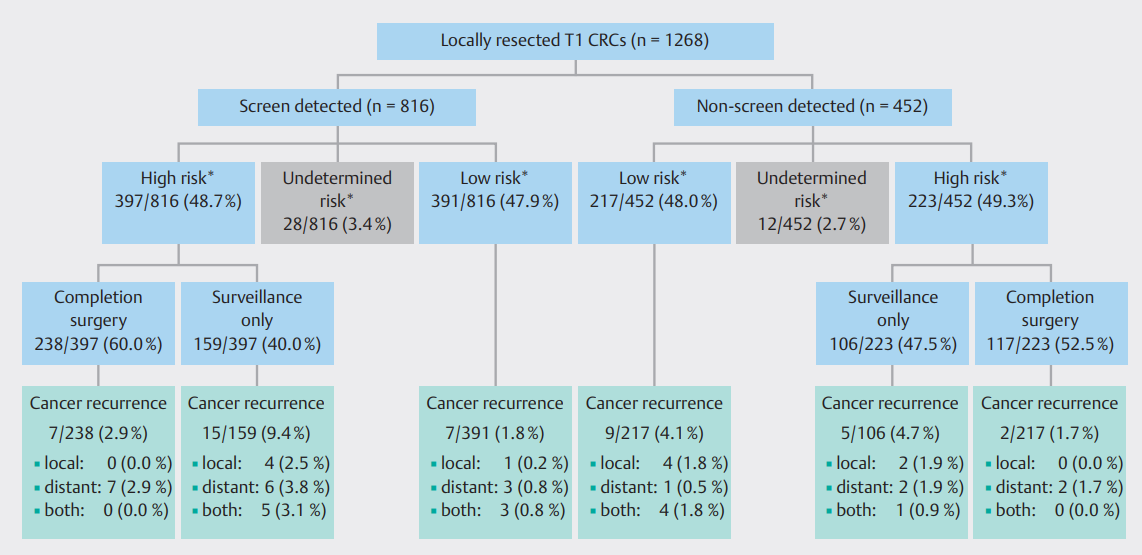
图2. 1268例内镜切除筛查和非筛查发现的T1结直肠癌(CRCs)的治疗策略和肿瘤结果,根据组织病理风险组细分。
TTR、MFS、CSS和整体生存
中位随访51个月(IQR 30个月)后,38/1114例筛查检测患者(3.4%)和24/689例未筛查检测患者(3.5%)发生CRC复发。在筛查检测患者中,19例(1.7%)死于CRC相关原因:随访期间癌症复发(n=13);诊断时远处转移(n=3);CRC治疗相关原因(n=3)。在未筛查检测组中,11例患者(1.6%)观察到CRC相关死亡,其中8例死于癌症复发后,3例死于CRC治疗相关原因。筛查检测到的T1 CRC患者中估计的3年和5年TTR与未筛查检测到的患者相似(调整后的风险比[HR] 1.05,95%CI 0.62-1.79)(图3a)。
筛查检测组32/38例癌症复发患者发现远处转移(84.2%),而非筛查检测组15/24例患者发现远处转移(62.5%)。两组在3和5岁时的MFS无显著差异(调整后HR 1.41,95%CI 0.75-2.65)(图3 b)。两组的估计3年和5年CSSs都很高,筛查检测和非筛查检测患者之间没有显著差异(调整后的HR 1.05,95%CI 0.47-2.34)(图3 c)。对三种治疗策略单独的肿瘤学结果的进一步分析没有显示任何一种策略的筛查检测和非筛查检测T1 CRCs之间癌症复发或CRC相关死亡的差异。
与癌症特异性结局相反,筛查检测到的T1 CRC人群的总生存率明显更高,3年和5岁时的总生存率分别为97.0%和91.9%,而非筛查检测到的T1 CRC患者的总生存率为87.4%和75.3%,即使根据诊断时的年龄、性别和ASA分类进行调整(调整后的HR 0.51,95%CI 0.38-0.68)(图3d)。

图3. 筛查检测和未筛查检测的T1结直肠癌(CRC)患者在以下方面的结局:a复发时间;b无转移生存期;c癌症特异性生存期;d总生存期。
讨论
在这项研究中,我们发现通过基于人群的筛查检测到的T1 CRCs与未筛查检测到的T1 CRCs相比,LNM、3年和5年TTR、MFS和CSS的比率具有可比性。此外,基于常规临床和组织学风险因素的LNM预测模型在两组之间的性能没有显著差异(AUROC 0.66 vs.60;P=0.47)。这些发现表明,当前基于未筛查检测到的T1 CRCs的风险分层模型也可以应用于筛查检测到的T1 CRCs。因此,筛查检测到的T1 CRCs和非筛查检测到的T1 CRCs之间不需要差别治疗。然而,筛查检测到的T1 CRC患者由于与CRC无关的死亡风险较低,总体生存率显着提高(调整后的HR 0.51,95%CI 0.38-0.68)。
本研究的结果并不支持我们的假设,即通过基于人群的筛查检测到的T1 CRCs与筛查计划之外的T1 CRCs之间可能存在分期分布和肿瘤结局差异。两组之间LNM的比例没有显著差异,观察到的LNM发生率与筛查计划实施前文献中报道的一致。
研究表明,筛查检测到的和未筛查检测到的T1 CRCs中,LNM和癌症复发的风险没有显著差异。在两组中观察到的LNM常规风险因素的可比表现以及TTR、MFS和CSS的相似率进一步证实,通过筛查检测到的T1 CRCs可以与筛查之外检测到的T1 CRCs进行类似的治疗。
欧洲消化内镜学会(ESGE)及其附属学会的官方期刊。
Endoscopy为关于胃肠道内窥镜检查的最新技术和国际发展的重要期刊。在国际编委会的专家指导下,本刊提供高质量的内容,以满足全球内窥镜医师、外科医生、临床医生和研究人员的需求。
Endoscopy每年出版12期,内容包括高质量的综述论文、原创论文、前瞻性研究、有价值的诊断和治疗进展调查、以及对最重要的国内和国际会议进行的深入报道。文章经常辅以在线视频内容。
在Endoscopy上出版的所有论文都经过严格的同行评审。基于在线投稿和快速处理,保证了电子版和印刷版的出版速度。
